- La tuberculosis es una infección bacteriana prevenible y curable que afecta sobre todo a los pulmones, pero puede dañar muchos otros órganos.
- Se transmite por vía aérea desde personas con enfermedad activa; la infección puede permanecer latente años y reactivarse si bajan las defensas.
- El diagnóstico combina pruebas rápidas moleculares, baciloscopia, cultivo y radiología; el tratamiento estándar usa varios antibióticos durante al menos 6 meses.
- La TB multirresistente y la coinfección con VIH complican el control, por lo que son esenciales la prevención, la vacunación infantil con BCG y la inversión sostenida en salud.
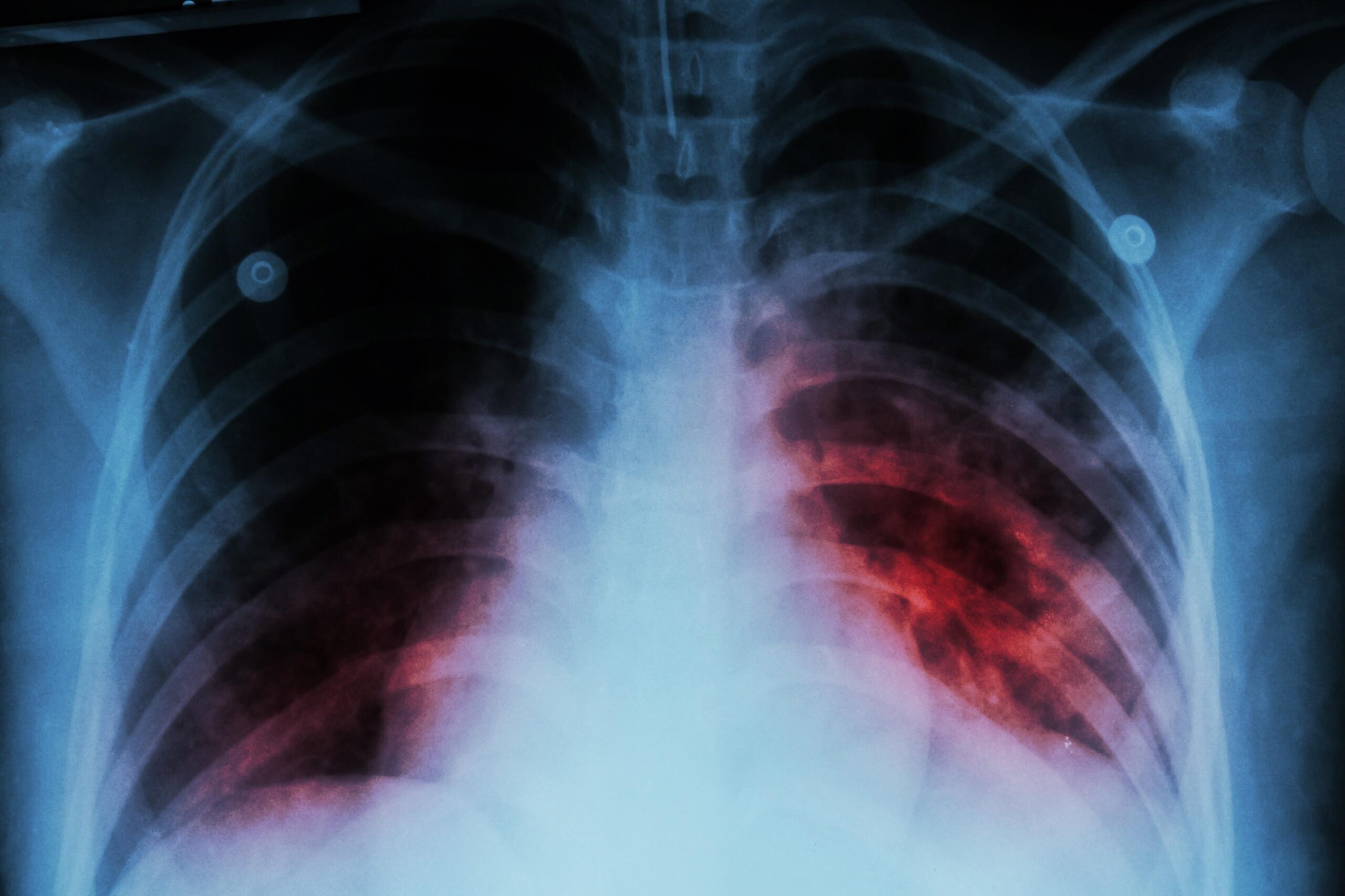
La tuberculosis sigue siendo, a día de hoy, una de esas enfermedades infecciosas que nunca terminan de irse. Aunque suene a algo del pasado, ligado a sanatorios de montaña y a la famosa “tisis”, la realidad es que continúa causando millones de contagios en todo el planeta y cientos de miles de muertes cada año. Pese a ello, es una enfermedad prevenible y curable si se diagnostica a tiempo y se trata correctamente.
Esta infección está provocada por una bacteria muy particular, el Mycobacterium tuberculosis o bacilo de Koch, capaz de mantenerse latente durante años sin dar la cara y reactivarse cuando el sistema inmunitario se debilita. Afecta sobre todo a los pulmones, pero puede aparecer prácticamente en cualquier órgano. Entender bien en qué consiste, cómo se contagia, qué síntomas da, cómo se diagnostica y qué tratamientos existen es clave tanto para los profesionales sanitarios como para cualquier persona que quiera cuidar su salud.
¿Qué es la tuberculosis y qué tipos existen?
La tuberculosis es una infección bacteriana crónica y contagiosa cuyo agente causal principal es Mycobacterium tuberculosis, aunque otras micobacterias como M. bovis, M. africanum, M. canetti o M. microti también pueden producirla, sobre todo en personas con defensas bajas. Tradicionalmente se la ha conocido como tisis, tisis pulmonalis o peste blanca, nombres que recuerdan lo devastadora que ha sido a lo largo de la historia.
El reservorio fundamental es el ser humano, y el órgano diana principal son los pulmones. No obstante, la bacteria puede colonizar pleura, meninges, ganglios linfáticos, sistema genitourinario, huesos, articulaciones, corazón, ojos, piel o incluso diseminarse por la sangre produciendo formas graves como la tuberculosis miliar. Por eso se diferencia entre formas pulmonares y extrapulmonares, y entre infección latente y enfermedad activa.
Cuando el bacilo entra en el organismo, lo habitual es que el sistema inmunitario logre contenerlo. En este caso hablamos de infección tuberculosa latente: la persona no tiene síntomas, no contagia y solo puede detectarse mediante pruebas inmunológicas como la tuberculina o los ensayos de liberación de interferón gamma.
Si el sistema de defensas fracasa en algún momento, el bacilo se reactiva, se multiplica y aparece la tuberculosis activa. Esta fase sintomática es la que puede transmitirse a otras personas, en especial cuando hay afectación pulmonar o laríngea, ya que la bacteria se expulsa al ambiente al toser, hablar, estornudar o escupir.
Dentro de la tuberculosis pulmonar, se describen habitualmente dos grandes escenarios clínicos: la tuberculosis primaria, que se desarrolla poco después de la infección inicial (más típica de la infancia y muchas veces con pocos síntomas) y deja un complejo primario característico en pulmón y ganglios, y la tuberculosis postprimaria o de reactivación, más agresiva, que suele aparecer años después en adolescentes o adultos y que es la forma clásica con tos crónica, hemoptisis y pérdida de peso.
Cómo se contagia la tuberculosis
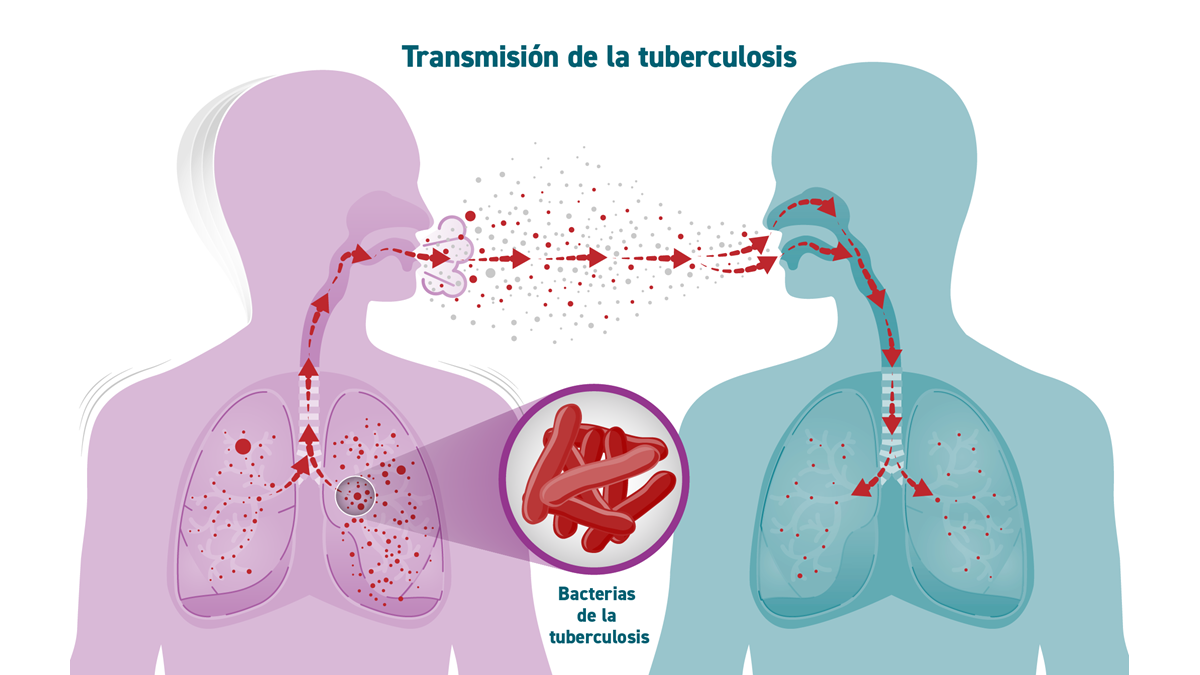
La única vía de transmisión relevante de la tuberculosis en la comunidad es la vía aérea. Las personas con enfermedad pulmonar activa expulsan al toser, estornudar, hablar o incluso cantar unas diminutas gotas cargadas de bacilos (gotas de Flügge o droplets) de entre 0,5 y 5 micrómetros de diámetro. Se calcula que un solo estornudo puede generar cientos de miles de estas partículas capaces de contener la bacteria.
Cualquier persona que respire ese aire contaminado en espacios cerrados y mal ventilados puede inhalar suficientes bacilos como para infectarse, ya que la dosis infectante es baja; incluso la inhalación de una sola bacteria viable podría, en teoría, dar lugar a infección. El riesgo de contagio aumenta con la proximidad, la duración del contacto, el número de bacilos expulsados, la virulencia de la cepa y la calidad de la ventilación del lugar.
Son especialmente vulnerables quienes tienen contactos prolongados, frecuentes o intensos con una persona bacilífera: convivientes, compañeros de trabajo en locales cerrados, pacientes y profesionales en entornos sanitarios, personas internas en prisiones, residentes y personal de centros sociosanitarios o personas que viven en refugios para personas sin hogar. Un enfermo con tuberculosis pulmonar activa no tratada puede infectar entre 10 y 15 personas cada año.
También existe una vía digestiva, hoy mucho menos frecuente, ligada al consumo de leche no pasteurizada procedente de vacas infectadas por Mycobacterium bovis. Esta forma fue importante históricamente, pero se ha reducido drásticamente con el control veterinario y la higienización de productos lácteos en muchos países.
La cadena de transmisión puede romperse aislando al paciente con tuberculosis pulmonar infecciosa y empezando cuanto antes un tratamiento antituberculoso eficaz. Transcurridas aproximadamente dos semanas de terapia correcta, la mayoría de los enfermos con cepas no resistentes dejan de contagiar, aunque las recomendaciones de aislamiento pueden variar según la situación clínica y los resultados bacteriológicos.
Qué ocurre en el organismo: de la infección latente a la enfermedad
Una vez inhalados, los bacilos de la tuberculosis alcanzan los alvéolos pulmonares, donde son fagocitados por los macrófagos. En una proporción importante de casos (alrededor del 30 %), estos macrófagos no logran destruirlos porque Mycobacterium tuberculosis bloquea la fusión entre el fagosoma y el lisosoma. El bacilo empieza entonces a multiplicarse en el interior de estas células.
Con el tiempo, el sistema inmunitario monta una respuesta organizada y se forman granulomas en los focos de infección: estructuras compuestas por macrófagos transformados, linfocitos y una zona central de necrosis caseosa donde pueden quedar bacilos en estado de latencia. Cuando la inmunidad celular madura, muchos de estos bacilos se eliminan y la carga bacteriana se mantiene a raya.
En esta fase, hablamos de infección tuberculosa latente: la persona no tiene síntomas, pero sus pruebas inmunológicas frente a la tuberculosis (como la intradermorreacción con PPD o los ensayos de liberación de interferón gamma) se positivizan. El individuo no contagia a nadie, aunque los bacilos que persisten en el tejido necrótico pueden reactivarse años más tarde si las defensas se debilitan.
La progresión desde la infección latente a la enfermedad tuberculosa activa se da en torno al 5-10 % de las personas infectadas a lo largo de su vida, pero este riesgo se dispara en presencia de inmunodeficiencias, especialmente por VIH, en pacientes tratados con fármacos inmunosupresores (como los anti-TNF usados en artritis reumatoide), en situaciones de desnutrición severa o ante enfermedades crónicas que deterioran la respuesta inmune.
En las personas con coinfección VIH y tuberculosis, el riesgo de reactivación puede aumentar un 10 % por año. Por eso se recomienda buscar activamente infección tuberculosa latente en estos pacientes y tratarla de forma preventiva con isoniacida u otros esquemas abreviados, para reducir la probabilidad de desarrollar tuberculosis activa.
Síntomas de la tuberculosis
En la infección latente no hay síntomas clínicos y la persona se encuentra bien, algo que contribuye a que la tuberculosis se mantenga como un problema silencioso a gran escala. El problema surge cuando se pasa a la fase de enfermedad activa, en la que los bacilos se multiplican de forma descontrolada y empiezan a dañar tejidos.
Los síntomas generales de la tuberculosis activa suelen ser insidiosos, progresan durante semanas o meses y se confunden con facilidad con otras patologías: fiebre prolongada (a menudo febrícula), cansancio, sensación de falta de energía, pérdida del apetito, adelgazamiento sin motivo claro, sudoración nocturna y, en estadios avanzados, dificultad para respirar.
Cuando la afectación principal está en los pulmones, lo más típico es la tos persistente que dura más de tres semanas, seca al principio y más tarde acompañada de expectoración, a veces con sangre (hemoptisis). Se suma dolor torácico opresivo o punzante, sobre todo al inspirar o toser, y en algunos casos disnea progresiva. Esta forma es la que más contagia porque el bacilo se encuentra en el esputo.
En niños y adolescentes, la tuberculosis puede tener una presentación más atípica, con fiebre prolongada, pérdida de peso y mal estado general, pero poca tos al inicio. En los lactantes, la enfermedad puede diseminarse con rapidez y producir formas graves como meningitis tuberculosa o tuberculosis miliar, de ahí la importancia de la vacunación con BCG en países de alta incidencia.
Hay que tener en cuenta que algunas personas con tuberculosis, especialmente en fases iniciales, pueden no notar síntomas llamativos y, sin embargo, estar transmitiendo el bacilo. Por eso, toda tos y expectoración de más de quince días, asociada a fiebre o pérdida de peso, debe hacer sospechar tuberculosis y ser estudiada.
Formas pulmonares y extrapulmonares
La forma más frecuente es la tuberculosis pulmonar, que se manifiesta como neumonía tuberculosa. En la infección primaria, típica de la infancia, aparece el llamado complejo de Ghon (foco pulmonar + linfangitis + adenitis parahiliar) y suele ser paucisintomática. En la reactivación del adulto, la clínica es más marcada, con tos crónica, esputo hemoptoico, sudores nocturnos y pérdida de peso; además, estos pacientes son altamente contagiosos y requieren aislamiento al menos durante las primeras dos semanas de tratamiento.
Otra forma torácica frecuente es la pleuritis tuberculosa, que aparece sobre todo en personas jóvenes, de forma aguda y generalmente unilateral. Se caracteriza por la acumulación de un exudado pleural con predominio de linfocitos y niveles elevados de adenosina desaminasa (ADA). Cursa con dolor pleurítico y dificultad respiratoria según la cantidad de líquido.
La tuberculosis extrapulmonar representa en torno al 10-20 % de los casos en personas inmunocompetentes, porcentaje que puede ascender hasta el 60 % en individuos con inmunodeficiencia, como ocurre en la infección por VIH. Aunque estas formas no suelen ser contagiosas por sí mismas, a menudo coexisten con afectación pulmonar, que sí supone un foco de transmisión.
Entre las localizaciones extrapulmonares destacan la tuberculosis meníngea (meningitis tuberculosa), con cefalea, rigidez de nuca y déficit neurológicos; la afectación del sistema nervioso central con tuberculomas cerebrales o medulares; la tuberculosis ocular (iris, cuerpos ciliares y coroides); la tuberculosis cardiovascular con pericarditis que puede evolucionar a pericarditis constrictiva; y la tuberculosis ganglionar, muy típica en niños y jóvenes, con grandes adenopatías cervicales que pueden fistulizar y dar lugar a escrofulodermia.
Otras formas son la tuberculosis genitourinaria, causa clásica de piuria estéril y de esterilidad por afectación de epidídimos o trompas de Falopio; la tuberculosis osteoarticular, que afecta huesos y articulaciones y puede originar osteomielitis o la conocida enfermedad de Pott cuando compromete la columna vertebral; y la tuberculosis intestinal, que se asocia a dolor abdominal crónico, diarrea y adelgazamiento.
Tuberculosis miliar y formas diseminadas
La tuberculosis miliar es una forma diseminada muy grave, consecuencia de la propagación hematógena masiva del bacilo, que siembra múltiples órganos y tejidos. Es más frecuente en personas de edad avanzada y en individuos con alteración severa del sistema inmunitario, especialmente pacientes con VIH avanzado, desnutrición marcada o tratamientos inmunosupresores intensivos.
Puede debutar de manera aguda, con fiebre alta, mal estado general y afectación multiorgánica, o de forma más insidiosa, con febrícula, sudoración, pérdida de peso y síntomas difusos. Para el diagnóstico se requieren habitualmente cultivos de esputo, orina, jugo gástrico o médula ósea, además de pruebas de imagen como radiografía o tomografía computarizada, que pueden mostrar el clásico patrón miliar.
En estos casos, el retraso diagnóstico y terapéutico aumenta notablemente la mortalidad, por lo que es fundamental mantener un alto grado de sospecha en pacientes inmunodeprimidos con fiebre prolongada de origen desconocido, incluso si la radiografía inicial es poco concluyente.
Factores de riesgo y población más vulnerable
La probabilidad de infección y de desarrollo de enfermedad tuberculosa no es la misma para todas las personas. Hay factores que incrementan claramente el riesgo, tanto de infectarse como de pasar de la infección latente a la enfermedad activa.
Entre los factores de riesgo de infección destacan vivir o trabajar en entornos con hacinamiento y mala ventilación (prisiones, refugios para personas sin hogar, centros residenciales, determinadas industrias), la convivencia con una persona con tuberculosis pulmonar activa, el trabajo en el ámbito sanitario en zonas de alta incidencia y el haber nacido o viajar con frecuencia a países donde la tuberculosis es muy común.
En cuanto al riesgo de progresar a enfermedad activa, la condición más importante a nivel mundial es la infección por VIH, que multiplica por más de 10 la probabilidad de enfermar. También aumentan el riesgo la diabetes mellitus, la desnutrición, el consumo nocivo de alcohol, el tabaquismo (sobre todo más de 20 cigarrillos al día), la insuficiencia renal crónica, el linfoma de Hodgkin, la enfermedad pulmonar obstructiva crónica y otras situaciones de inmunodepresión.
La dieta puede jugar un papel modulador. En algunos estudios realizados en inmigrantes del subcontinente indio residentes en Londres, se observó un mayor riesgo de tuberculosis en personas con dietas muy restrictivas, posiblemente relacionado con déficits de micronutrientes como la vitamina D, la vitamina B12 o el hierro. La malnutrición grave, que sigue siendo una realidad en determinadas regiones del mundo, empeora notablemente la respuesta inmunitaria y favorece el desarrollo de tuberculosis activa.
Datos epidemiológicos señalan también desigualdades raciales y sociales: por ejemplo, en ciertos países la tasa de tuberculosis es significativamente más alta en personas negras o afroamericanas no hispanas en comparación con personas blancas no hispanas, lo que refleja el impacto del acceso desigual a la atención sanitaria, la pobreza y el hacinamiento.
Magnitud del problema: datos mundiales recientes
La tuberculosis continúa figurando entre las principales causas de muerte por enfermedad infecciosa en el mundo. En 2024 se estima que 10,7 millones de personas enfermaron de tuberculosis, con una distribución aproximada de 5,8 millones de hombres, 3,7 millones de mujeres y 1,2 millones de niños. Ese mismo año murieron alrededor de 1,23 millones de personas por esta enfermedad, de las cuales unas 150 000 estaban coinfectadas por VIH.
Se calcula que alrededor de una cuarta parte de la población mundial ha estado en contacto con el bacilo de la tuberculosis y presenta infección latente, aunque solo entre un 5 y un 10 % desarrollará enfermedad activa a lo largo de su vida. La carga se concentra sobre todo en países de ingresos bajos y medianos, donde se registran más del 80 % de los casos y las muertes.
En 2024, la mayor parte de los nuevos diagnósticos se produjo en la Región de Asia Sudoriental de la OMS, seguida por la del Pacífico Occidental y la de África. Ocho países concentran aproximadamente dos tercios de los casos mundiales: India, Indonesia, Filipinas, China, Pakistán, Nigeria, República Democrática del Congo y Bangladesh. El peso económico de la enfermedad es enorme, con cerca del 50 % de las personas tratadas y sus familias sufriendo gastos considerados catastróficos (más del 20 % de la renta familiar).
La tuberculosis asociada a la resistencia a los antimicrobianos agrava aún más el panorama. Solo dos de cada cinco personas con tuberculosis farmacorresistente tuvieron acceso a tratamiento adecuado en 2024. Pese a todo, se estima que las actividades de prevención, diagnóstico y tratamiento implementadas desde el año 2000 han salvado alrededor de 83 millones de vidas en todo el mundo.
Diagnóstico de la tuberculosis
El diagnóstico de la tuberculosis combina la valoración clínica con pruebas de imagen y de laboratorio. La OMS recomienda que, ante cualquier persona con síntomas sospechosos (tos de más de dos o tres semanas, fiebre prolongada, pérdida de peso, sudoración nocturna), se utilicen como primer paso pruebas diagnósticas rápidas, preferentemente moleculares, capaces de detectar el material genético del bacilo y, en muchos casos, su resistencia a los fármacos de primera línea.
Entre estas pruebas se incluyen los ensayos moleculares automatizados y otros test con biomarcadores aplicables en el lugar de atención, que ofrecen resultados iniciales en menos de 48 horas. Han supuesto un gran avance para identificar precozmente casos de tuberculosis y de tuberculosis resistente a medicamentos, especialmente en entornos con pocos recursos.
La bacteriología clásica sigue siendo, no obstante, la herramienta de referencia: la baciloscopia de esputo mediante tinción de Ziehl-Neelsen o auramina permite visualizar bacilos ácido-alcohol resistentes (BAAR). Es una técnica barata, rápida y eficaz para detectar a los pacientes más contagiosos, con una sensibilidad cercana al 70-80 % en las formas pulmonares con alta carga bacteriana.
El cultivo en medios específicos, como el Löwenstein-Jensen (a base de huevo, verde de malaquita, glicerol y asparagina), ofrece mayor sensibilidad, permite identificar la especie y realizar estudios de sensibilidad a fármacos. Su principal limitación es el crecimiento muy lento de M. tuberculosis, que puede tardar entre 30 y 90 días. Métodos más recientes, como el MODS (susceptibilidad a drogas mediante observación microscópica), acortan tiempos y evalúan de forma simultánea la resistencia a isoniacida y rifampicina.
El diagnóstico de la infección tuberculosa latente se realiza mediante la prueba de la tuberculina (test de Mantoux, donde se inyecta intradérmicamente PPD, un derivado proteico purificado del bacilo) o mediante ensayos de liberación de interferón gamma y nuevas pruebas cutáneas con antígenos específicos. Un resultado positivo indica contacto previo con el bacilo, pero no diferencia entre infección latente y enfermedad activa, por lo que debe interpretarse junto a los hallazgos clínicos y radiológicos.
La radiografía de tórax es esencial en la valoración de la tuberculosis pulmonar. Suele mostrar lesiones apicales, cavitaciones, infiltrados en segmentos posteriores y otras alteraciones sugerentes. En casos complejos, se recurre a tomografía computarizada, resonancia magnética (sobre todo en afectación neurológica) o ecografía (para pleura, ganglios o abdomen). Además, en todo paciente diagnosticado de tuberculosis se recomienda ofrecer prueba de VIH, dado el fuerte vínculo entre ambas infecciones.
Tratamiento de la tuberculosis sensible
La tuberculosis es una enfermedad curable en la gran mayoría de los casos, siempre que se disponga de antibióticos adecuados y que el paciente cumpla estrictamente el tratamiento. El esquema clásico se basa en la combinación de varios fármacos de primera línea, administrados durante un mínimo de 6 meses, para evitar la selección de bacilos resistentes.
Los medicamentos básicos son la isoniacida, rifampicina, pirazinamida y etambutol (a veces estreptomicina). Suele establecerse una primera fase intensiva de dos meses, en la que se utilizan los cuatro fármacos, seguida de una fase de continuación con dos de ellos (habitualmente isoniacida y rifampicina) durante cuatro meses más. En algunos casos, según la localización o el estado inmunitario, puede ser necesario prolongar la terapia.
Es fundamental que el paciente tome todas las dosis tal y como se le ha indicado, sin interrumpir el tratamiento por su cuenta aunque se encuentre mejor. Suspenderlo antes de tiempo o hacerlo de forma irregular favorece la proliferación de bacilos resistentes y puede hacer que la enfermedad empeore rápidamente. En ocasiones se recurre a la terapia directamente observada, en la que un profesional sanitario supervisa la toma de la medicación para asegurar la adherencia.
En las primeras semanas, especialmente si el paciente tiene tuberculosis pulmonar bacilífera, se aconseja que permanezca en casa o incluso hospitalizado para reducir el riesgo de contagio, y que aplique medidas de higiene respiratoria: cubrirse la boca al toser, usar mascarilla en espacios compartidos, ventilar bien el domicilio y evitar el contacto cercano con personas no expuestas.
Los fármacos de primera línea se clasifican como antituberculosos principales por su elevada potencia y eficacia, mientras que los de segunda línea (cicloserina, etionamida, fluoroquinolonas, entre otros) se reservan para casos con resistencia o intolerancia. La elección precisa del esquema y su duración la determina el especialista en función de la situación clínica, los resultados de sensibilidad y la presencia de comorbilidades.
Tuberculosis multirresistente (TB-MDR) y ultrarresistente (XDR)
Uno de los retos más graves en el control global de la tuberculosis es la resistencia a los antibióticos. La tuberculosis multirresistente (TB-MDR) se define como aquella causada por cepas de M. tuberculosis resistentes al menos a rifampicina e isoniacida, los dos pilares del tratamiento de primera línea. La tuberculosis ultrarresistente (XDR) va más allá, añadiendo resistencia a cualquier fluoroquinolona y al menos a un fármaco de segunda línea inyectable o de los considerados clave.
La farmacorresistencia suele aparecer cuando los fármacos antituberculosos se usan mal: prescripción incorrecta (dosis inadecuadas o combinaciones insuficientes), mala calidad de los medicamentos, interrupción temprana del tratamiento o incumplimiento por parte del paciente. Una vez seleccionadas, las cepas resistentes pueden transmitirse a otras personas, generando cadenas de contagio difíciles de cortar.
El diagnóstico de TB-MDR requiere confirmación bacteriológica mediante pruebas moleculares rápidas que detectan mutaciones de resistencia o mediante cultivo con estudio de sensibilidad. La OMS recomienda esquemas terapéuticos basados en combinaciones orales de nueva generación, que buscan reducir la duración del tratamiento y mejorar la tolerancia.
En 2022 se priorizaron regímenes abreviados de seis meses como los esquemas BPaLM (bedaquilina, pretomanid, linezolid y moxifloxacino) y BPaL (bedaquilina, pretomanid y linezolid) para determinados perfiles de pacientes, así como combinaciones con bedaquilina, delamanid, linezolid, levofloxacino y clofazimina. Estos tratamientos, administrados exclusivamente por vía oral, han mostrado alta eficacia y una importante reducción del número de comprimidos y del tiempo total de terapia.
A pesar de estos avances, la cobertura sigue siendo insuficiente: solo una fracción de las personas con TB-MDR o resistente a rifampicina accede a estos esquemas novedosos. Además, los fármacos de segunda línea son más caros y presentan más efectos secundarios, lo que obliga a una monitorización estrecha por parte del equipo sanitario. En algunos casos seleccionados, se puede ofrecer profilaxis con levofloxacino a contactos de pacientes con TB-MDR para tratar de evitar la progresión a enfermedad.
Relación entre tuberculosis y VIH
La interacción entre tuberculosis y VIH es especialmente peligrosa. Las personas infectadas por el VIH tienen una probabilidad aproximadamente 12 veces mayor de desarrollar enfermedad tuberculosa que quienes son VIH-negativas. La tuberculosis es, de hecho, una de las principales causas de muerte entre los pacientes con VIH, y la coinfección acelera la progresión de ambas patologías.
En 2024, unas 150 000 personas murieron por tuberculosis asociada al VIH. La mayoría de estos casos se concentraron en la Región de África de la OMS, donde la prevalencia de VIH es muy alta. Aunque el 82 % de las personas que enfermaron de tuberculosis en ese año se sometieron a una prueba de detección de VIH, solo alrededor del 61 % de quienes tenían coinfección recibieron tratamiento antirretroviral, cifra aún lejos de lo deseable.
Desde 2004, la OMS promueve actividades conjuntas TB/VIH: cribado bidireccional (probar TB en personas con VIH y VIH en enfermos de TB), prevención y tratamiento de la infección tuberculosa latente, inicio temprano de terapia antirretroviral, mejora del acceso al diagnóstico y medidas de control de la infección en centros sanitarios. Se calcula que la expansión del tratamiento de la tuberculosis y del tratamiento antirretroviral desde 2005 ha evitado casi 10 millones de muertes relacionadas con la coinfección.
Prevención y medidas de control
La prevención de la tuberculosis se basa en tres grandes pilares: detectar precozmente los casos activos y tratarlos de forma completa, proteger a las personas con mayor riesgo de progresión mediante tratamiento de la infección latente y utilizar intervenciones de salud pública como la vacunación y las medidas de control ambiental.
A nivel individual, se recomienda buscar atención médica si se presentan síntomas sospechosos como tos prolongada, fiebre sin causa aparente y pérdida de peso. Cuanto antes se diagnostique y se trate al paciente, menor será el tiempo durante el que puede contagiar a otros y mayores serán las posibilidades de curación sin secuelas graves.
En personas con alto riesgo (infectados por VIH, contactos estrechos de enfermos con tuberculosis activa, pacientes inmunodeprimidos, etc.) se aconseja realizar pruebas para detectar infección tuberculosa latente y, si son positivas, valorar tratamiento preventivo. Completar el esquema profiláctico prescrito es esencial para reducir la probabilidad de pasar a enfermedad activa.
Las medidas de higiene respiratoria son muy importantes: las personas con tuberculosis deben cubrirse la boca y la nariz al toser o estornudar, usar mascarilla en espacios compartidos, desechar correctamente los pañuelos y esputos, lavarse las manos después de toser y mantener una buena ventilación en el hogar y en lugares públicos. En centros sanitarios y otros entornos de riesgo, es crucial un diseño adecuado de la ventilación y el uso de equipos de protección respiratoria para el personal.
En el ámbito familiar y comunitario, se recomiendan medidas adicionales como restringir las visitas de personas no expuestas durante las primeras semanas de tratamiento del enfermo, asegurar que se toman todas las dosis prescritas, evitar el humo del tabaco y otras sustancias irritantes y mejorar, en lo posible, la situación nutricional de los convivientes.
Vacunas frente a la tuberculosis: BCG y nuevas estrategias
La vacuna más conocida frente a la tuberculosis es la BCG (Bacillus Calmette-Guérin), desarrollada en el Instituto Pasteur entre 1905 y 1921 y utilizada de forma masiva a partir de la posguerra. Se trata de una cepa viva atenuada derivada de Mycobacterium bovis, que se administra normalmente en los primeros meses de vida en países con alta incidencia de la enfermedad.
La BCG ofrece una protección muy notable frente a las formas graves de tuberculosis en la infancia, como la meningitis tuberculosa o la tuberculosis miliar, con una eficacia que ronda el 80 % en menores de 4 años. Sin embargo, su eficacia frente a la tuberculosis pulmonar del adolescente y del adulto es mucho más variable, con cifras que oscilan entre el 0 y el 80 % según el contexto epidemiológico y los estudios realizados.
En países con baja incidencia, como España, la vacunación sistemática con BCG en recién nacidos se abandonó en torno a 1980, optándose por su uso selectivo en grupos de riesgo concretos. En cambio, muchos países de renta baja y media mantienen la vacunación universal infantil como parte esencial de sus programas de control de la tuberculosis.
En los últimos años se han desarrollado nuevas aproximaciones vacunales. Entre ellas destaca RUTI, una vacuna terapéutica diseñada para acortar el tratamiento de la infección tuberculosa latente de nueve a un mes de isoniacida, y MTBVAC, la primera vacuna experimental basada en un bacilo humano de tuberculosis atenuado (en contraste con la BCG, que es de origen bovino). Esta última, desarrollada por un grupo de investigación de la Universidad de Zaragoza en colaboración con la farmacéutica Biofabri, ha mostrado en ensayos iniciales una protección superior a la de BCG en modelos preclínicos.
Aunque estas vacunas todavía están en fase de desarrollo o de evaluación clínica, suponen una esperanza de futuro para mejorar el control de la tuberculosis, especialmente en países de alta carga, y podrían complementar o sustituir a la BCG en determinadas poblaciones si demuestran seguridad y eficacia suficientes.
Impacto económico y respuesta internacional
Controlar la tuberculosis requiere no solo esfuerzos sanitarios, sino también inversiones económicas sostenidas. Para alcanzar los objetivos globales fijados en la reunión de alto nivel de Naciones Unidas sobre tuberculosis de 2023, se estima que se necesitan alrededor de 22 000 millones de dólares anuales destinados a prevención, diagnóstico, tratamiento y atención.
En 2024, cerca del 82 % del gasto en servicios relacionados con la tuberculosis en países de ingresos bajos y medianos procedió de fuentes nacionales. Brasil, China, India, la Federación de Rusia y Sudáfrica concentraron la mayor parte de este esfuerzo, destinando más de 3000 millones de dólares, lo que supone dos tercios del total de fondos nacionales invertidos en estos países. La financiación internacional, por su parte, se mantuvo relativamente estable, en torno a 1100 millones de dólares anuales.
El panorama es aún más ajustado en lo que respecta a investigación e innovación en tuberculosis. En 2023 se invirtieron unos 1200 millones de dólares, lejos del objetivo global de 5000 millones anuales. Este déficit de financiación retrasa el desarrollo de nuevas herramientas diagnósticas, fármacos y vacunas, y dificulta la implantación de estrategias más eficaces en los países de mayor carga.
La Organización Mundial de la Salud colabora estrechamente con los gobiernos, organizaciones internacionales y sociedad civil para impulsar la respuesta global: elabora guías y recomendaciones, apoya la implantación de programas nacionales de control, promueve la vigilancia epidemiológica, fomenta la investigación y coordina iniciativas para ampliar el acceso al diagnóstico rápido y a los nuevos esquemas de tratamiento, especialmente en tuberculosis multirresistente.
Todas estas acciones persiguen avanzar hacia las metas de la Estrategia “Fin a la Tuberculosis” y de los Objetivos de Desarrollo Sostenible, que aspiran a reducir drásticamente la incidencia y la mortalidad asociadas a esta enfermedad y a eliminar los gastos catastróficos para las familias afectadas.
Todas estas acciones persiguen avanzar hacia las metas de la Estrategia “Fin a la Tuberculosis” y de los Objetivos de Desarrollo Sostenible, que aspiran a reducir drásticamente la incidencia y la mortalidad asociadas a esta enfermedad y a eliminar los gastos catastróficos para las familias afectadas.
La tuberculosis, pese a ser una enfermedad conocida desde hace milenios y para la que disponemos de antibióticos eficaces, continúa siendo un importante problema de salud pública mundial. La combinación de diagnóstico precoz, tratamientos completos y bien supervisados, medidas de prevención, vacunación en contextos de alta incidencia e inversión sostenida en sistemas de salud y en investigación es la clave para romper de forma definitiva la cadena de transmisión y evitar que millones de personas sigan sufriendo una infección que hoy, con las herramientas adecuadas, es prevenible y curable.

