- Las áreas terapéuticas en oncología se organizan en unidades multidisciplinares con protocolos específicos y medicina personalizada.
- La oncología concentra gran parte de la I+D farmacéutica, con foco en tumores complejos y terapias de precisión.
- Las terapias dirigidas actúan sobre alteraciones moleculares concretas, mejoran la eficacia y reducen el daño a células sanas.
- La investigación básica, traslacional y los ensayos clínicos sostienen la innovación y el acceso a nuevos tratamientos oncológicos.
Las áreas terapéuticas en oncología se han convertido en uno de los ejes centrales de la medicina moderna. No solo hablamos de tipos de cáncer o de tratamientos aislados, sino de auténticas estructuras de trabajo que integran diagnóstico, terapias avanzadas, investigación y seguimiento del paciente de una forma coordinada. Cada vez más centros oncológicos organizan su actividad en torno a áreas específicas que agrupan a profesionales de diferentes especialidades para tomar decisiones conjuntas y ofrecer una atención realmente personalizada.
Al mismo tiempo, la industria farmacéutica y biotecnológica está volcando una parte enorme de sus recursos en la investigación oncológica, con especial foco en tumores difíciles de tratar y en pacientes con pocas opciones terapéuticas. Desde las terapias dirigidas basadas en el perfil genómico del tumor, hasta los programas de cáncer hereditario y los ensayos clínicos internacionales, todas estas piezas encajan en un mismo puzzle: frenar el cáncer, prolongar la supervivencia y mejorar la calidad de vida de las personas que lo padecen.
Qué son las áreas terapéuticas en oncología y cómo se organizan
En los grandes centros oncológicos actuales, la atención al cáncer ya no se organiza simplemente por servicios clásicos (oncología médica, radioterapia, cirugía, etc.), sino por áreas o unidades multidisciplinares centradas en cada tipo de tumor. Un ejemplo claro es el modelo del Cancer Center de la Clínica Universidad de Navarra, que estructura su asistencia por tumores en catorce áreas diferentes que funcionan en paralelo en sus dos sedes.
Cada una de estas áreas multidisciplinares reúne a los profesionales y servicios implicados en todo el proceso oncológico: oncólogos médicos, radiooncólogos, cirujanos, radiólogos, anatomopatólogos, especialistas en medicina nuclear, enfermería oncológica, psicooncología, genética, farmacología, entre otros. El objetivo es que, desde el primer momento, todos los expertos necesarios participen en el diseño del plan de diagnóstico y tratamiento de cada paciente concreto.
Estas áreas celebran de forma periódica sesiones clínicas multidisciplinares (a menudo conocidas como comités de tumores), en las que se revisan los casos, se actualizan los diagnósticos, se valora la respuesta a los tratamientos y se adoptan decisiones de manera consensuada. Este enfoque colaborativo reduce la variabilidad, integra la evidencia científica más reciente y garantiza que el paciente no dependa de la visión aislada de un único especialista.
A nivel organizativo, cada área dispone de protocolos asistenciales específicos que marcan las rutas diagnósticas, los criterios de indicación de tratamientos y el seguimiento posterior. Estos protocolos se actualizan de forma constante con los resultados de la investigación básica y traslacional, la experiencia clínica acumulada y los datos de ensayos internacionales. Además, suelen incluir indicadores de calidad y seguridad para evaluar resultados y detectar oportunidades de mejora.
Otro pilar clave de estas áreas es la medicina personalizada. En la práctica, esto significa que para cada tumor (y en muchos casos para cada paciente) se integra un programa propio de diagnóstico molecular avanzado, biomarcadores, estudios genéticos de predisposición familiar cuando está indicado y acceso a terapias dirigidas y ensayos clínicos específicos. En aquellas áreas en las que existe sospecha de componente hereditario, se añaden programas de cáncer hereditario con unidades de consejo genético para familias de riesgo.
Para completar el círculo, muchas unidades mantienen un registro retrospectivo de casos que permite estudiar la evolución de los pacientes, comparar resultados, identificar patrones y generar hipótesis para nuevas líneas de investigación. Esta cultura de datos y análisis continuo es la que impulsa, en buena parte, las mejoras progresivas en supervivencia y calidad de vida.
Principales áreas terapéuticas y el papel de la oncología
Si miramos el mapa global de la industria farmacéutica y biotecnológica, la oncología es solo una de las grandes áreas terapéuticas estratégicas, aunque probablemente la que concentra una mayor parte de la inversión en I+D. Muchas compañías estructuran su investigación en torno a bloques como: enfermedades cardiovasculares y metabólicas, oncología, patologías respiratorias, inflamación y autoinmunidad, infecciones y vacunas, y neurociencia.
En ese contexto, la oncología ocupa un lugar prioritario. Hay empresas que destinan más del 70 % de su presupuesto de investigación y desarrollo exclusivamente a proyectos oncológicos, con la idea de abordar necesidades no cubiertas en tumores sólidos complejos y en enfermedades oncohematológicas. El foco está especialmente puesto en cánceres avanzados, tumores poco frecuentes o asociados a mutaciones genéticas concretas, en los que los tratamientos convencionales ofrecen resultados limitados.
Un ejemplo representativo es el compromiso de compañías como Servier, que han hecho de la oncología una prioridad estratégica desde hace años. Su trabajo se centra en pacientes con escasas opciones terapéuticas, incluyendo cáncer colorrectal avanzado, tumores de páncreas, gliomas, cáncer de vías biliares y leucemias como la leucemia linfoblástica aguda, tanto en adultos como en población pediátrica. El objetivo es desarrollar terapias capaces de controlar la enfermedad durante más tiempo y mejorar el pronóstico de tumores de muy mala evolución.
Esta apuesta se traduce en el desarrollo de tratamientos dirigidos y medicina de precisión que actúan sobre alteraciones moleculares concretas del tumor. Para ello, se combinan capacidades de investigación interna con una intensa red de colaboraciones externas: centros de referencia como el de Boston o la biotecnológica Symphogen en Dinamarca, alianzas con laboratorios, start-ups biotecnológicas y grupos académicos. En conjunto, se pueden llegar a mantener decenas de asociaciones de investigación orientadas a acelerar la llegada de terapias innovadoras a la práctica clínica.
En paralelo, otras áreas terapéuticas también juegan un papel relevante en la salud pública. La investigación en enfermedades cardiovasculares y cardiometabólicas ha dado lugar a hitos clave en diabetes tipo 2 y enfermedad cardiovascular. De igual modo, el desarrollo de vacunas ha sido, durante más de un siglo, una de las grandes historias de éxito en medicina preventiva, ayudando a evitar millones de casos de enfermedades infecciosas como el sarampión, la polio o el virus del papiloma humano.
La irrupción de la COVID-19 mostró hasta qué punto las compañías con experiencia en vacunas y enfermedades infecciosas pueden reaccionar con rapidez. Desde el inicio de la pandemia, muchas se volcaron en diseñar vacunas, terapias y estrategias de prevención frente al SARS-CoV-2, apoyándose en su experiencia previa en VIH, ébola y otras infecciones graves. Todo este bagaje repercute también en oncología, porque tecnologías como el ARN mensajero o los vectores virales tienen aplicaciones directas en tratamientos oncológicos avanzados.
Tipos de tratamiento del cáncer dentro de las áreas terapéuticas
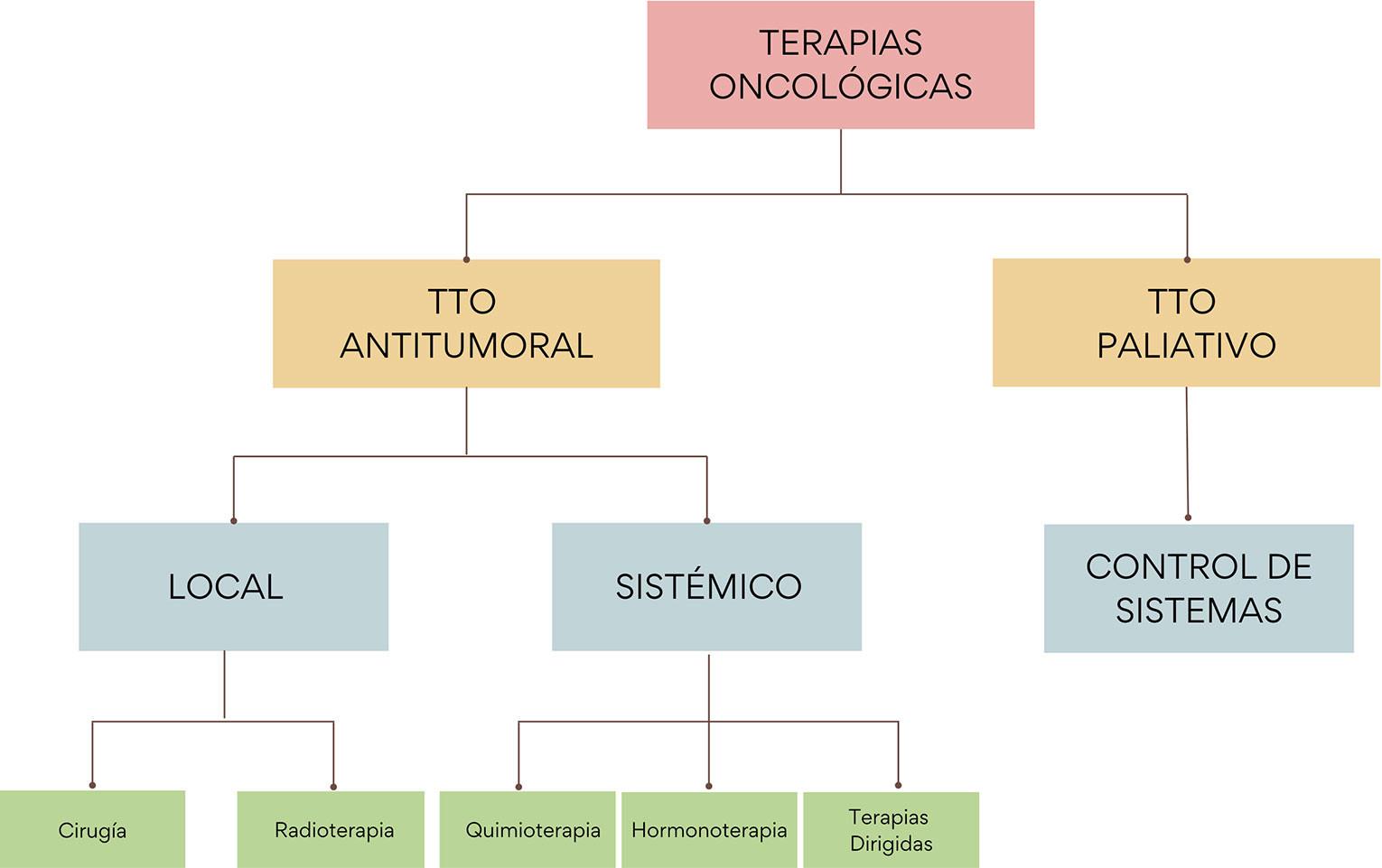
En el día a día del paciente, las áreas terapéuticas en oncología se traducen en planes de tratamiento combinados que utilizan distintas estrategias según el tipo de cáncer, su extensión y las características individuales de la persona. Aunque algunas personas solo cuentan con una opción terapéutica disponible, lo habitual es que el manejo del cáncer incluya varias modalidades a lo largo del tiempo.
Entre los tratamientos clásicos destacan:
- Cirugía oncológica, orientada a extirpar el tumor y, cuando es posible, lograr la curación o reducir la masa tumoral.
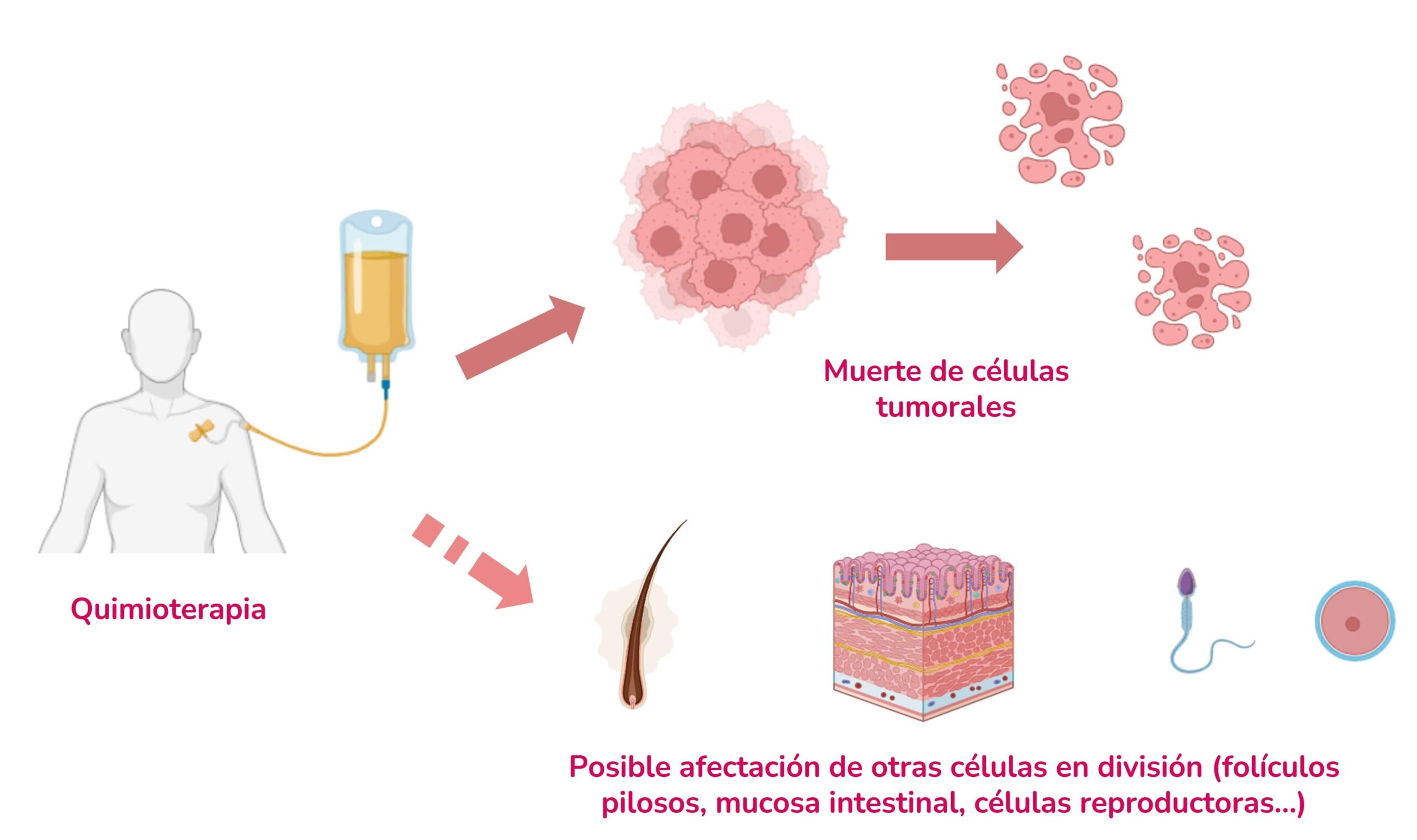
- Quimioterapia, basada en fármacos citotóxicos que destruyen células tumorales o frenan su proliferación, aunque también pueden dañar células sanas.
- Radioterapia, que emplea radiación de alta energía para destruir células cancerosas de forma localizada.
Estos enfoques pueden combinarse entre sí (por ejemplo, cirugía seguida de quimioterapia y radioterapia) o con terapias más modernas como la inmunoterapia o las terapias dirigidas, dependiendo de la situación clínica. El tipo de tratamiento, la secuencia y la intensidad se definen en el seno de las áreas terapéuticas, teniendo en cuenta la mejor evidencia disponible y el estado general del paciente.
Para cada tipo de tumor existen guías y protocolos específicos que recogen los tratamientos de elección según estadio, presencia de metástasis, mutaciones moleculares, edad del paciente y comorbilidades. Por eso, cuando una persona recibe un diagnóstico de cáncer, es habitual que el equipo médico recomiende consultar información más detallada sobre ese tipo concreto de cáncer, ya sea en adultos o en población infantil, ya que las indicaciones pueden variar ampliamente.
Además, es muy recomendable que el paciente prepare una lista de preguntas para el médico centradas en las opciones de tratamiento: qué alternativas hay, qué objetivos persigue cada una (curativa, paliativa, control de síntomas), posibles efectos secundarios, duración del tratamiento, necesidad de hospitalización, impacto en la vida diaria, etc. Esa conversación es clave para tomar decisiones informadas y ajustadas a las preferencias y valores de cada persona.
En los últimos años, junto a estos tratamientos clásicos, han cobrado un enorme protagonismo las terapias dirigidas y la inmunoterapia, que forman parte de la revolución de la medicina de precisión. Estas nuevas estrategias se integran en las áreas terapéuticas como parte esencial del arsenal terapéutico, especialmente en tumores con alteraciones moleculares claras y en pacientes que se benefician de abordajes personalizados.
Terapias dirigidas: una de las grandes esperanzas en oncología
Las terapias dirigidas son tratamientos farmacológicos diseñados para actuar de forma muy específica sobre las moléculas o vías de señalización que están detrás del desarrollo y progresión de un determinado tumor. En lugar de atacar de forma indiscriminada a todas las células que se dividen rápido (como ocurre con mucha quimioterapia clásica), estos fármacos se enfocan en dianas concretas implicadas en el cáncer.
El objetivo principal de este tipo de terapias es bloquear el crecimiento y la diseminación de las células tumorales. Por eso también se las conoce como fármacos molecularmente dirigidos o terapias molecularmente dirigidas. Están pensadas para interferir en funciones clave de la célula cancerosa: señales de proliferación, mecanismos de reparación del ADN, formación de nuevos vasos sanguíneos (angiogénesis), procesos de invasión y metástasis, entre otros.
Desde el punto de vista práctico, las terapias dirigidas se aplican directamente sobre la molécula o la vía alterada que está impulsando el tumor en un paciente concreto. Esto hace que, en muchos casos, su eficacia sea superior a la de los tratamientos convencionales cuando se administran en el contexto adecuado. Además, al actuar de forma más selectiva sobre las “células malas”, las células sanas que las rodean sufren un daño menor, lo que se traduce en perfiles de efectos secundarios diferentes y, a menudo, más tolerables.
Para poder utilizar una terapia dirigida, antes hay que saber qué alteraciones genómicas presenta el tumor. Aquí entra en juego el estudio del ADN mediante técnicas de secuenciación genómica. A través de estas pruebas, los investigadores y clínicos identifican cambios, mutaciones o reordenamientos genéticos que explican por qué se ha desarrollado ese tumor y qué mecanismos lo mantienen activo.
En este contexto, se habla mucho de medicina personalizada o medicina de precisión. La idea es sencilla pero potente: ya no tratamos “un tipo de cáncer” de forma genérica, sino el tumor exacto de cada paciente, con su perfil molecular propio. Gracias a las tecnologías de secuenciación, es posible conocer con gran detalle qué alteraciones están presentes en el ADN tumoral y, a partir de ahí, seleccionar la terapia dirigida que mejor encaje con esas dianas.
La secuenciación genómica permite definir lo que se conoce como perfil genómico del paciente. En ese perfil se recoge información exhaustiva sobre las secuencias de ADN relevantes para el tumor, identificando las mutaciones clave que pueden convertirse en dianas terapéuticas. Cuanto más precisas son estas técnicas, más fino es el ajuste entre el fármaco y la alteración molecular, lo que se traduce en diagnósticos más exactos y tratamientos más eficaces.
A día de hoy, las terapias dirigidas se han ido incorporando al tratamiento de un número creciente de tumores: cáncer de mama con determinadas mutaciones, cáncer de pulmón no microcítico con alteraciones en EGFR, ALK o ROS1, tumores gastrointestinales, melanoma, algunos cánceres hematológicos, entre otros. En muchos casos, estos fármacos han cambiado por completo el pronóstico de enfermedades que, hace no tanto, tenían opciones muy limitadas.
Una vez que los equipos de expertos detectan cuál es la molécula dañada o la vía de señalización alterada, se diseña una estrategia terapéutica específica. Las terapias dirigidas suelen agruparse en dos grandes categorías: fármacos de molécula pequeña y anticuerpos monoclonales.
- Fármacos de molécula pequeña: son compuestos químicos que, por su tamaño reducido, pueden entrar en el interior de la célula y bloquear proteínas o enzimas clave implicadas en el crecimiento del tumor. Muchos inhibidores de tirosina kinasa (ITK) entran en esta categoría.
- Anticuerpos monoclonales: son proteínas diseñadas para reconocer de manera muy específica una molécula diana, habitualmente situada en la superficie de las células tumorales o en su entorno. Pueden bloquear directamente esa diana, marcar la célula para que el sistema inmunitario la destruya o llevar consigo fármacos o toxinas que se liberan en el tumor.
Al centrarse de forma preferente en las células tumorales o en su microambiente, estas terapias producen, en general, un daño menor sobre los tejidos sanos en comparación con algunos tratamientos tradicionales. Eso no significa que estén libres de efectos secundarios, pero sí que su toxicidad puede ser más manejable y, en muchos casos, más específica (por ejemplo, alteraciones cutáneas, digestivas o cardiovasculares concretas).
Con el paso de los años y el avance de la investigación oncológica, las terapias dirigidas se han ido consolidando como pilar de tratamiento en un número creciente de áreas terapéuticas. Gracias a ellas, en muchos pacientes el cáncer se controla durante periodos prolongados, y determinados tumores que antes eran rápidamente mortales pueden llegar a manejarse como enfermedades crónicas en algunos casos.
Además, la velocidad a la que evolucionan las técnicas de secuenciación genómica hace que cada vez sea posible identificar dianas terapéuticas más precisas. Esto abre la puerta a tratamientos todavía más personalizados, en los que la combinación de distintos fármacos dirigidos y la adaptación continua a las resistencias que desarrolla el tumor se convierten en estrategias habituales.
Investigación, ensayos clínicos y colaboración global
El progreso en las áreas terapéuticas en oncología no sería posible sin una investigación intensa y sostenida que va desde el laboratorio básico hasta los ensayos clínicos en pacientes. La investigación básica busca desentrañar los mecanismos íntimos por los que las células normales se transforman en células cancerosas: qué mutaciones se acumulan, cómo se alteran las vías de señalización, de qué manera escapan al sistema inmunitario, etc.
A partir de estos hallazgos se impulsa la investigación traslacional, cuyo objetivo es trasladar lo descubierto en el laboratorio a posibles aplicaciones clínicas: nuevas dianas terapéuticas, biomarcadores para seleccionar pacientes, combinaciones de fármacos más eficaces, estrategias para superar resistencias, entre otras. Muchos de los avances en terapias dirigidas, inmunoterapia o combinaciones de tratamiento surgen precisamente de esta interacción continua entre ciencia básica y práctica clínica.
Los ensayos clínicos son la pieza clave para demostrar que una nueva terapia es segura y eficaz. Se llevan a cabo en fases sucesivas (I, II, III y, en ocasiones, IV) y permiten evaluar diferentes dosis, comparaciones frente a tratamientos estándar, combinaciones y secuencias de administración. Las áreas terapéuticas en oncología suelen estructurar una cartera de ensayos activa, de modo que los pacientes que cumplen criterios puedan acceder a fármacos innovadores antes de su aprobación general.
En este campo, la colaboración internacional es imprescindible. Ningún centro ni ninguna compañía puede abarcar por sí sola toda la complejidad del cáncer. De ahí que existan redes de colaboración entre hospitales, grupos cooperativos, universidades, biotecnológicas y grandes farmacéuticas. Es frecuente que una empresa mantenga decenas de acuerdos con socios distintos repartidos por todo el mundo, coordinando estudios clínicos, compartiendo plataformas tecnológicas y cruzando datos de investigación.
Todo este ecosistema tiene un objetivo común: acelerar el desarrollo de tratamientos innovadores que realmente marquen la diferencia para los pacientes. A medida que se van aprobando más terapias dirigidas, inmunoterapias y combinaciones inteligentes, las áreas terapéuticas en oncología deben adaptarse para integrar esas opciones de manera ordenada, garantizando que los pacientes correctos reciban el tratamiento adecuado en el momento oportuno.
En paralelo, también crece la importancia de la calidad de vida como resultado clínico fundamental. No basta con prolongar la supervivencia; se busca que la persona pueda mantener su actividad, su autonomía y su bienestar emocional el máximo tiempo posible. Por eso, muchos programas oncológicos incluyen unidades de cuidados de soporte, psicooncología, rehabilitación, manejo del dolor y seguimiento a largo plazo, integradas en estas mismas áreas terapéuticas.
Todo este entramado de áreas multidisciplinares, medicina personalizada, terapias dirigidas, ensayos clínicos y colaboración global está transformando la forma de tratar el cáncer. Aunque queda mucho camino por recorrer y todavía hay tumores de muy mal pronóstico, la combinación de ciencia revolucionaria, organización clínica y enfoque centrado en la persona está logrando que, para un número creciente de pacientes, el cáncer se convierta en una enfermedad más controlable y, en algunos casos, crónica, con expectativas de vida y calidad impensables hace apenas unas décadas.