- La luz puede organizarse en estados cuánticos exóticos como luz líquida y supersólidos de polaritones, con propiedades de fluido y sólido a la vez.
- La espectroscopía se basa en la interacción luz-materia bajo la aproximación dipolar para revelar niveles de energía y reglas de selección en átomos y moléculas.
- Los colores, brillos y transparencias cotidianas se explican por la respuesta oscilatoria de los electrones y la dispersión, absorción y reflexión de la luz.
- Desde el cielo azul hasta los metales brillantes, los mismos principios físicos muestran cómo la luz revela la estructura y dinámica de la materia en todas las escalas.

La luz es mucho más que lo que percibimos con los ojos: es una herramienta de investigación, un material cuántico exótico, un fluido que puede comportarse como un sólido y, además, el hilo conductor que explica por qué el cielo es azul, por qué una hoja es verde o por qué un metal brilla. Cuando hablamos de “luz como elemento revelador de la materia” nos referimos precisamente a todo eso: a cómo la radiación electromagnética nos permite ver, medir, excitar y, en algunos casos, incluso construir nuevos estados de la materia.
En las últimas décadas, la física y la óptica cuántica han dado un salto espectacular. No solo hemos aprendido a usar la luz para estudiar átomos, moléculas y materiales, sino que hemos conseguido doblarla a nuestra voluntad hasta hacer que se comporte como un líquido sin fricción o como un cristal, abrir la puerta a los supersólidos de luz y a nuevas tecnologías cuánticas. Este artículo recorre, con calma pero a fondo, cómo interactúa la luz con la materia, qué estados extraños pueden surgir de esa interacción y cómo todo esto se conecta con los colores cotidianos, la espectroscopía y los dispositivos que juegan con sombras, reflejos y apariciones luminosas.
De la luz líquida a los supersólidos: cuando los fotones se comportan como materia
Uno de los hallazgos más llamativos de la física contemporánea es que la luz, que solemos imaginar como algo intangible y sin masa, puede organizarse colectivamente y comportarse como si fuera un fluido, o incluso como un sólido que al mismo tiempo fluye sin rozamiento. Esto rompe totalmente la intuición clásica, pero se entiende bien dentro del marco de la mecánica cuántica y de las quasipartículas.
En 2002, el físico Humberto Michinel, de la Universidad de Vigo, descubrió mediante simulaciones numéricas en medios ópticos fuertemente no lineales que la luz podía “condensarse” de manera muy parecida a un líquido. A este fenómeno se le llamó luz líquida y fue reconocido por el American Institute of Physics como uno de los diez grandes descubrimientos de aquel año. Sin embargo, durante un tiempo fue solo una predicción teórica: hubo que esperar a 2013 para observar la primera luz líquida experimentalmente en un gas de átomos de sodio extremadamente fríos.
Poco después, varios laboratorios internacionales demostraron que era posible recrear un comportamiento de luz líquida a temperatura ambiente. Equipos del Instituto de Nanotecnología en Lecce, el Politécnico de Montreal, la Universidad Aalto y el Imperial College lograron que la luz se comportara como un superfluido utilizando dispositivos ópticos especiales y láseres ultrarrápidos. Estas configuraciones permiten que los fotones se acoplen fuertemente con el medio material, dando lugar a quasipartículas híbridas llamadas polaritones.
Los polaritones son mezclas cuánticas de fotones y excitaciones del medio, por ejemplo electrones ligados o excitones. Una buena forma de imaginarlos es la analogía del esquiador que baja por nieve polvo: el esquiador sería la partícula principal y la nube de nieve la “cola” de interacciones que la acompaña. Físicamente, no es una partícula fundamental nueva, sino una descripción eficaz de un sistema complejo (luz + materia) que se comporta como si fuera una sola entidad con propiedades propias.
En algunos de estos montajes, los polaritones se organizan en lo que se conoce como condensado de Bose-Einstein de fotones o de quasipartículas, donde un gran número de bosones ocupan el mismo estado cuántico. A temperaturas cercanas al cero absoluto o, de forma efectiva, en sistemas ópticos con pérdidas y bombeo adecuados, los fotones adquieren un comportamiento colectivo similar al de un fluido cuántico: pueden fluir sin viscosidad, sortear obstáculos sin disipar energía y mostrar superfluidez.
El siguiente paso, aún más sorprendente, ha sido la realización experimental de supersólidos de luz. Un supersólido es una fase de la materia en la que las partículas están dispuestas en una estructura cristalina, como en un sólido ordinario, pero al mismo tiempo el sistema es superfluido: puede fluir sin fricción. Es decir, la materia presenta simultáneamente orden espacial (como la red de átomos de un cristal de sal) y fluidez sin viscosidad.
Un equipo del Consejo Nacional de Investigación de Italia (CNR), con científicos como Dimitris Trypogeorgos y Daniele Sanvitto, logró generar un estado supersólido formado por polaritones de luz. Para ello reemplazaron los átomos ultrafríos típicos de otros experimentos por un semiconductor de arseniuro de aluminio y galio con un patrón de crestas nanométricas y un láser que excitaba la muestra. La combinación de la estructura del semiconductor, que restringe el movimiento y los niveles de energía de las quasipartículas, con la luz láser dio lugar a un patrón polaritónico con simetría cristalina y superfluidez simultánea.
Medir este tipo de sistema no es nada trivial: nunca antes se había evaluado experimentalmente un supersólido de luz. El equipo tuvo que caracterizar con enorme precisión la fase, la distribución espacial y el flujo sin rozamiento de estos polaritones atrapados. Aun así, las ventajas potenciales son enormes. Un supersólido basado en luz es más fácil de manipular que uno hecho de átomos, y se perfila como plataforma para nuevos materiales cuánticos con aplicaciones en computación cuántica, sensores ultraprecisos, materiales ligeros y resistentes para aeroespacio y automoción, e incluso dispositivos energéticos de alta conductividad.
En palabras de los propios investigadores, se trata solo del comienzo de una nueva familia de materiales luminosos con propiedades difíciles de imaginar desde la intuición clásica. Nos encontramos, literalmente, ante una materia de luz que abre un abanico inmenso de posibilidades tecnológicas y conceptuales.
Luz líquida, superfluidez y condensados de Bose-Einstein
Para comprender mejor lo que está pasando en estos experimentos, conviene recordar qué es la superfluidez y cómo se relaciona con los condensados de Bose-Einstein (CBE). En los años treinta del siglo XX se descubrió que el helio, al enfriarlo por debajo de unos -271 °C, mostraba un comportamiento radicalmente distinto: su conductividad térmica se disparaba y su viscosidad se hacía prácticamente nula.
En este régimen, el helio-4 (un bosón, al tener número entero de espín) se convierte en un superfluido: no ofrece resistencia a fluir, puede trepar por las paredes de un recipiente y escaparse por orificios ridículamente pequeños. El helio-3, que es un fermión, necesita temperaturas aún más bajas para alcanzar un estado análogo, y lo hace mediante mecanismos cooperativos que lo convierten efectivamente en un sistema de pares de bosones.
Fritz London propuso en 1938 que la superfluidez es un ejemplo macroscópico de un condensado de Bose-Einstein, un estado cuántico de la materia predicho por Bose y Einstein en 1925. En un CBE, todas las partículas bosónicas comparten una única función de onda macroscópica, de forma que el sistema se comporta como una “superpartícula” coherente. Esto explica por qué aparecen propiedades tan extrañas como la superfluidez o la superconductividad.
La conexión entre estos fenómenos y la luz líquida no es trivial, pero está clara la analogía: cuando se consiguen condensados de fotones o de polaritones, los fotones dejan de ser simples cuantos de campo electromagnético que van a su aire y se comportan de forma coherente como si fueran materia. Se han logrado condensados de Bose-Einstein de fotones en cavidades ópticas, donde la luz rebota entre espejos y se thermaliza gracias a la interacción con un medio, ocupando preferentemente el modo de baja energía.
Una de las grandes preguntas abiertas es de naturaleza fundamental: ¿qué nos dice exactamente la luz líquida sobre la dualidad onda-partícula de la luz? ¿Estamos viendo fotones individuales que fluyen como un líquido o un estado colectivo que es a la vez intermedio entre la descripción ondulatoria y la corpuscular? Resolver estas cuestiones podría cambiar nuestra comprensión de la naturaleza de la radiación y llevar a nuevas revoluciones tecnológicas, como dispositivos ópticos basados en superfluidez de luz o arquitecturas de computación cuántica fotónica más robustas.
La luz como herramienta para revelar el mundo microscópico: espectroscopía
Más allá de estos estados exóticos, la aplicación más extendida de la luz en ciencia es la espectroscopía. En química, física y biología, la manera estándar de averiguar qué niveles de energía tiene una molécula, un átomo o un sólido consiste en estudiar cómo absorbe o emite radiación electromagnética.
En un experimento de absorción típico se utiliza una fuente de luz (por ejemplo, una lámpara o un láser) y un monocromador, que descompone la luz en sus diferentes frecuencias o longitudes de onda. El monocromador se puede imaginar como un prisma o una red de difracción: a partir de un haz blanco separa cada “color” en una dirección diferente, permitiendo medir la intensidad de cada componente por separado.
Primero se registra el espectro de referencia de la fuente, es decir, la intensidad emitida en cada frecuencia antes de atravesar la muestra. Luego se hace pasar la luz por la sustancia que queremos estudiar y se mide de nuevo la intensidad por frecuencia. Al comparar ambos espectros (restando la señal con muestra a la de referencia) se obtiene el espectro de absorción: los “dientes” o picos indican qué frecuencias son absorbidas, y con qué intensidad.
Si en lugar de medir la luz que atraviesa la muestra se recoge la radiación emitida en otras direcciones, se puede obtener un espectro de emisión o de fluorescencia. Tanto la absorción como la emisión revelan las diferencias de energía entre niveles cuánticos del sistema (electrónicos, vibracionales, rotacionales, etc.), por lo que la espectroscopía es una especie de “tomografía energética” de la materia.
En la descripción cuántica, la materia se trata con mecánica cuántica mientras que la luz puede aproximarse clásicamente como un campo electromagnético oscilante. Esto simplifica mucho las cosas sin perder las características esenciales de la interacción. A intensidades de laboratorio, el campo eléctrico de la luz es débil en comparación con los campos internos de la molécula, por lo que se puede tratar como una perturbación sobre el Hamiltoniano molecular, que describe la energía electrónica y nuclear.
Radiación electromagnética, escalas y aproximación dipolar
La radiación electromagnética está compuesta por campos eléctrico y magnético que oscilan en el espacio y en el tiempo, perpendiculares entre sí y a la dirección de propagación: es una onda transversal. Sus ecuaciones de movimiento se derivan de las ecuaciones de Maxwell, y sus soluciones son ondas caracterizadas por una frecuencia angular ω y una longitud de onda λ.
Cuando una molécula se encuentra inmersa en este campo oscilante, sus electrones y núcleos “sienten” una fuerza periódica. En principio habría que resolver la ecuación de Schrödinger incluyendo explícitamente el campo electromagnético, algo inabordable para sistemas reales si no hacemos algunas aproximaciones razonables. La primera es que el efecto del campo magnético es mucho más débil que el del campo eléctrico en la mayoría de situaciones espectroscópicas, por lo que se suele despreciar.
La segunda simplificación clave es la llamada aproximación dipolar. Las longitudes de onda de la luz en rangos típicos (visible, infrarrojo, ultravioleta cercano) van desde decenas de nanómetros hasta milímetros, mientras que el tamaño de una molécula suele ser del orden de 1 nanómetro. Esto significa que, a escala molecular, el campo eléctrico se puede considerar casi uniforme: la onda es tan “larga” que la variación del campo entre un extremo y otro de la molécula es despreciable.
Matemáticamente, esto equivale a tomar el vector de onda q = 2π/λ como prácticamente cero a escala del sistema, de forma que el potencial vectorial y el campo se aproximan como homogéneos en todo el volumen molecular. En esta aproximación, la interacción luz-materia se reduce a un acoplamiento entre el dipolo eléctrico molecular y el campo externo. El Hamiltoniano de interacción radiación-materia queda entonces proporcional al producto del dipolo por el campo eléctrico.
Una vez fijados estos ingredientes, se utiliza teoría de perturbaciones dependiente del tiempo, en particular la regla de oro de Fermi, para calcular la probabilidad de que el sistema pase de un estado inicial i a un estado final f al absorber (o emitir) un fotón de determinada energía. Esa probabilidad es proporcional al cuadrado del elemento de matriz del operador dipolar entre ambos estados, lo que conecta directamente con las llamadas reglas de selección.
Reglas de selección: qué transiciones son visibles y cuáles están prohibidas
Las reglas de selección espectroscópicas nos dicen qué transiciones entre niveles cuánticos pueden observarse mediante absorción o emisión de luz en un experimento óptico. No basta con que exista una diferencia de energía adecuada entre dos estados: el elemento de matriz del dipolo de transición debe ser distinto de cero.
Desde el punto de vista de la simetría, esto se formula en términos de representaciones irreducibles (irreps) del grupo de simetría de la molécula o el cristal. El operador posición (o el momento dipolar) es impar respecto a la inversión espacial, es decir, cambia de signo al invertir las coordenadas. Por tanto, solo las transiciones entre estados de paridad opuesta (g ↔ u) pueden dar lugar a un elemento de matriz dipolar no nulo en sistemas con centro de inversión. Transiciones entre estados con la misma paridad (g → g o u → u) están prohibidas en dipolo eléctrico.
En términos vibracionales, si un modo normal es par (gerade), todos sus niveles (etiquetados por el número cuántico vibracional ν) comparten esa paridad; si es impar (ungerade), el estado fundamental y los excitados con ν par son pares, mientras que los niveles con ν impar son impares. Esto implica que modos vibracionales de tipo gerade no serán activos en espectroscopía de absorción infrarroja, mientras que modos ungerade sí darán lugar a bandas observables.
Para las rotaciones moleculares, el elemento de matriz de transición involucra los armónicos esféricos YJ,M, que describen los estados del momento angular. Para que una molécula pueda acoplarse al campo eléctrico y rotar, debe tener un momento dipolar permanente en su geometría de equilibrio. Por eso, los espectros rotacionales puros solo se observan en moléculas polares: los gases homonucleares como N2 u O2 no muestran líneas rotacionales en el infrarrojo puro.
Además, la conservación del momento angular impone que el número cuántico de rotación J solo puede cambiar en ±1 en una transición de dipolo eléctrico. Esto genera una serie de líneas igualmente espaciadas en energía, cuya intensidad depende tanto del elemento de matriz como de la población térmica de los niveles implicados. A temperatura ambiente, la energía térmica kBT es suficiente para poblar varios niveles rotacionales, de manera que el espectro muestra un conjunto de líneas cuya intensidad crece hasta un máximo (alrededor de cierto Jmax) y luego decrece.
En las transiciones vibracionales, si se aproxima cada modo a un oscilador armónico, la regla de selección básica es Δν = ±1: el cambio en el número cuántico vibracional entre estados inicial y final debe ser de una unidad. Esto haría que, idealmente, cada modo activo en infrarrojo produjera una sola línea de absorción a la frecuencia característica del modo. En la práctica, la anharmonicidad y el acoplamiento entre modos generan bandas adicionales y sobretonos, pero la idea de fondo es que la intensidad de las líneas está íntimamente ligada a la simetría y a la naturaleza del dipolo de transición.
Del átomo al objeto cotidiano: cómo la luz revela color, brillo y transparencia
Hasta ahora hemos hablado de la luz como herramienta de laboratorio, pero exactamente los mismos principios gobiernan lo que vemos cada día: por qué el cielo es azul, por qué una hoja es verde, por qué una nube es blanca o por qué un metal brilla como un espejo. Todo ello se reduce a cómo vibran los electrones cuando el campo eléctrico de la luz los sacude.
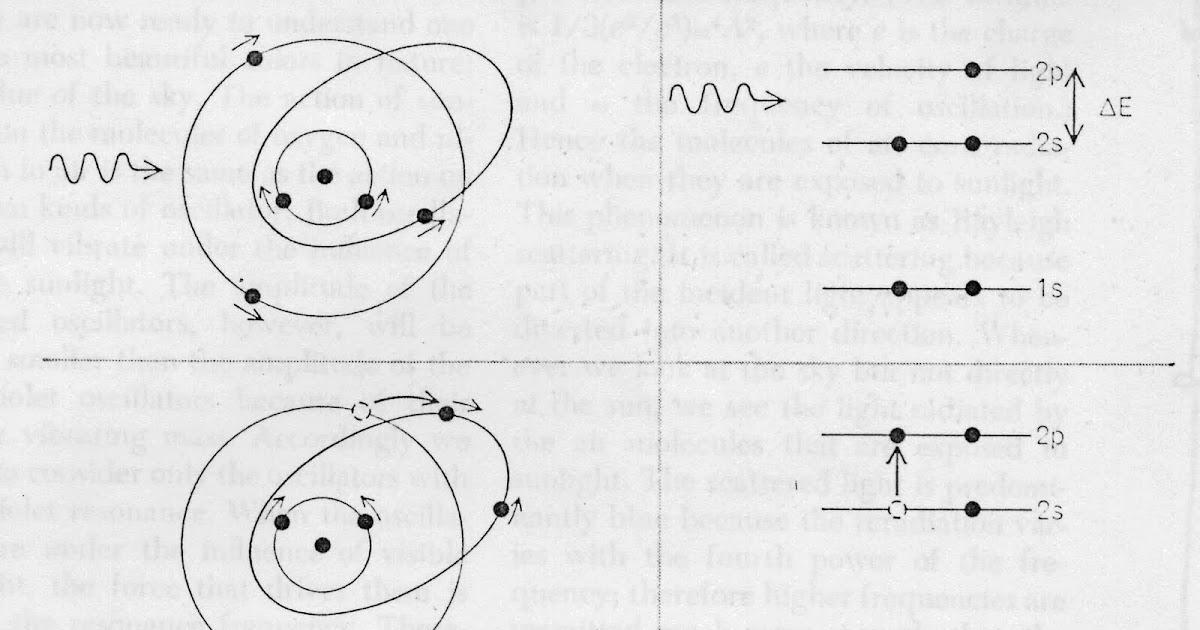
La teoría cuántica nos dice que la energía de la luz viene paquetizada en fotones, y que los átomos y moléculas solo pueden ocupar niveles de energía discretos. En el modelo más sencillo, un fotón con una energía que coincide exactamente con la diferencia entre dos niveles puede ser absorbido y excitar el átomo, que luego emitirá otro fotón al relajarse. Esta imagen por “saltos cuánticos” sirve para transiciones resonantes muy bien definidas, como las líneas espectrales de un gas diluido.
Sin embargo, los colores y brillos de los objetos habituales no provienen casi nunca de procesos estrictamente resonantes. En la mayoría de los sólidos y líquidos a temperatura ambiente, la luz visible tiene energías que no encajan exactamente con las transiciones electrónicas discretas de átomos aislados, y además los estados excitados se desexcitan sobre todo convirtiendo la energía en calor y no en fotones. Para describir esta situación de manera eficaz, se usa un modelo clásico de osciladores electrónicos.
En ese modelo, cada electrón ligado se representa como un oscilador armónico con una frecuencia de resonancia propia ω0, como si estuviera unido por un muelle al núcleo. Si aplicamos un campo eléctrico de frecuencia ω (la luz incidente), el electrón oscila a esa frecuencia forzada, no a la suya propia. La amplitud y la fase de la oscilación dependen de la relación entre ω y ω0: muy por debajo de la resonancia la respuesta es débil pero casi en fase, en resonancia la amplitud se dispara y la fase se desajusta 90 grados, y muy por encima la respuesta vuelve a ser pequeña y desfasada 180 grados.
Cada uno de estos osciladores emite a su vez radiación: una carga acelerada siempre emite luz. La intensidad de esa reradiación crece con la cuarta potencia de la frecuencia (ω4), de modo que, a igualdad de amplitud, las frecuencias más altas se dispersan mucho más intensamente que las bajas. Esto es justo lo que explica el color azul del cielo a través de la dispersión Rayleigh: las moléculas de aire (N2, O2) tienen resonancias electrónicas en el ultravioleta, pero la luz visible que las agita provoca una oscilación casi uniforme cuya reradiación crece fuertemente hacia el azul.
En un gas como el aire, donde las moléculas están distribuidas de forma casi aleatoria, las ondas reemitidas por cada oscilador se suman incoherentemente en la mayoría de direcciones: la intensidad total es simplemente la suma de las intensidades individuales. Por eso el cielo se ve azul cuando miramos lejos del Sol: lo que vemos es luz solar desviada por el aire, con predominio de las frecuencias altas. El fenómeno inverso da lugar al color rojizo del atardecer, cuando la luz ha atravesado una gran masa de aire y los azules han sido dispersados preferentemente fuera del haz directo.
En líquidos y sólidos, en cambio, los átomos o moléculas están arreglados de manera mucho más ordenada, y las ondas reemitidas tienden a interferir de forma coherente. En el interior del material, las radiaciones de cada oscilador se suman para formar una única onda refractada que avanza dentro del medio con una velocidad distinta de c (la de la luz en el vacío). Esta onda refractada es el origen del índice de refracción: la razón n = c/v mide cuánto “se frena” la luz al entrar en el material.
En una interfaz (por ejemplo, entre aire y vidrio o aire y agua), una fina capa de osciladores cercana a la superficie contribuye a la onda reflejada: la radiación hacia atrás desde esa región no queda cancelada completamente por interferencia y emerge como la luz que vemos rebotar en el vidrio o en la superficie del agua. Debido a la dependencia entre el número de osciladores coherentes y la longitud de onda, la intensidad total reflejada resulta prácticamente independiente de la frecuencia en el rango visible, de modo que el reflejo es blanco si la luz incidente es blanca.
Este mismo razonamiento explica por qué el agua pura o el vidrio son prácticamente incoloros: gran parte de la luz se refracta y atraviesa el material sin sufrir absorción significativa en el visible, porque sus resonancias fuertes están en el infrarrojo y en el ultravioleta. El material solo muestra un ligero tinte azulado-verdoso debido a una débil absorción en la zona roja del espectro: tras decenas de metros de recorrido, la componente roja se atenúa y predomina la luz verde-azul que llega a mayor profundidad.
Nubes blancas, papel, pigmentos y metales: la paleta completa de la luz
Las nubes parecen blancas porque están formadas por miles de millones de gotitas de agua de tamaño mayor que la longitud de onda de la luz. Cada gotita es un pequeño “grano” transparente que refleja y refracta la luz de forma similar a un cristal minúsculo de agua. La luz solar entra, se refleja varias veces en las interfaces entre aire y agua, se refracta, y sale en todas direcciones sin preferencia por ningún color concreto. El resultado es una mezcla de todas las longitudes de onda: blanco.
Si los granos o partículas dispersoras son mucho más pequeños que la longitud de onda (humo muy fino, polvo diminuto, gotículas casi evaporadas), el comportamiento se vuelve más parecido al de un gas: la dispersión tipo Rayleigh domina y aparece un tinte azulado, como se observa en el humo de cigarro o en nubes que se deshilachan en un día seco.
El papel ordinario está hecho de fibras de celulosa translúcidas, una maraña irregular de pequeños cilindros transparentes. La luz penetra en esa red, se refracta dentro de cada fibra y se refleja repetidamente en las distintas interfaces fibras-aire hasta que, finalmente, vuelve a salir hacia el observador. Como estas fibras no tienen resonancias en el visible, no absorben selectivamente y la luz que regresa es de nuevo una mezcla de todos los colores: el papel se ve blanco. El mismo razonamiento sirve para la nieve, la sal o el azúcar granulados: compuestos transparentes convertidos en conjuntos de pequeños cristalitos con múltiples reflexiones internas.
Cuando añadimos pigmentos o tintes a un material, lo que hacemos es introducir moléculas o iones con transiciones electrónicas en el rango visible. Los llamados colorantes orgánicos suelen ser sistemas con anillos conjugados y electrones deslocalizados que pueden moverse sobre distancias mayores, lo que reduce la energía de excitación y coloca las resonancias en el visible. Los iones metálicos con capas d o f parcialmente llenas también pueden tener niveles electrónicos a la distancia de energía adecuada para absorber regiones concretas del espectro visible.
En un pigmento rojo, por ejemplo, la banda de absorción cubre casi todo el visible salvo la zona roja: se absorben azules, verdes y amarillos y se refleja (o se transmite) preferentemente la componente roja. De manera parecida, un pigmento verde absorberá rojos y violetas, dejando pasar sobre todo las longitudes de onda intermedias. Como el material está en fase condensada, los niveles energéticos se ensanchan en bandas, de modo que la absorción no es una línea estrecha sino una franja relativamente amplia de frecuencias.
En objetos como vidrios coloreados (emplomados), los pigmentos se incorporan en la matriz vítrea. Cuando la luz incide, una parte se refleja en la superficie del vidrio igual que en un vidrio incoloro, con un ligero refuerzo en las frecuencias cercanas a las resonancias del pigmento. La fracción de luz que penetra experimenta absorción preferencial: solo sobreviven las longitudes de onda que el pigmento no absorbe. Por eso, vistos a contraluz, los vitrales muestran colores intensísimos y muy puros: la luz que llega al ojo es la que ha atravesado todo el espesor, filtrada espectralmente por el pigmento.
En una hoja de papel pintada o teñida, la luz entra en las fibras impregnadas de colorante, y tras múltiples pasadas una parte importante de la componente absorbida se ha convertido en calor. Lo que logra escapar y vuelve hacia el observador está dominado por las longitudes de onda que el pigmento no absorbe. Las plantas funcionan igual: las células vegetales contienen clorofila y otros pigmentos que absorben en azul y rojo, reflejando y transmitiendo sobre todo el verde. Las flores, con diferentes combinaciones de pigmentos, construyen la enorme variedad de colores que vemos en jardines y bosques.
Los objetos negros son aquellos que absorben prácticamente toda la luz incidente en todo el rango visible. El grafito, la brea o ciertas superficies tratadas están llenos de estructuras que atrapan la luz mediante múltiples reflexiones internas, con pérdidas en cada rebote hasta que apenas nada regresa. Un truco clásico de laboratorio consiste en apilar navajas o filos muy juntos: aunque los materiales sean brillantes, la luz que penetra entre ellos queda atrapada y se convierte en calor tras muchos recorridos, dando lugar a una apariencia casi perfectamente negra.
Los metales, por su parte, deben su brillo característico a la presencia de electrones de conducción casi libres. En un metal típico cada átomo aporta uno o varios electrones que no están ligados a un átomo concreto, sino que forman un “gas electrónico” que se extiende por toda la red cristalina. Estos electrones responden al campo eléctrico de la luz como osciladores de frecuencia muy baja, básicamente como cargas libres.
Cuando la luz visible incide en un metal, los electrones de conducción vibran en fase opuesta al campo, generando un campo inducido que cancela el campo incidente en el interior: no se forma una onda refractada significativa siempre que la frecuencia de la luz sea menor que la llamada frecuencia de plasma del metal (que suele estar en el ultravioleta). Como consecuencia, la energía de la onda luminosa no penetra en profundidad y se refleja casi toda en una finísima capa superficial cuyo grosor es inferior a 10-7 m.
Esto explica por qué metales como plata o aluminio son espejos casi perfectos en el visible: reflejan prácticamente el 100 % de la luz incidente, con una dependencia muy débil de la frecuencia. En metales coloreados, como el oro o el cobre, los electrones ligados que no forman parte del gas de conducción tienen resonancias en el azul-violeta, donde absorben parte de la luz. El resultado es que las componentes azules se atenúan y el reflejo dominante es amarillento-rojizo, dando lugar al color cálido característico de estos metales.
En el extremo opuesto, algunos materiales presentan fluorescencia: re-emiten luz a frecuencias más bajas que las absorbidas, tras relajar internamente parte de la energía. Esto se ve en pigmentos fluorescentes, minerales bajo luz ultravioleta o señales de seguridad. Aquí la luz no solo revela la materia, sino que la materia transforma activamente la radiación y nos devuelve información en otra región del espectro.
Al conectar estas distintas escalas —desde el supersólido de luz hasta la sombra que cambia de tamaño al mover una linterna sobre un objeto— vemos que la luz actúa siempre como un elemento revelador de la materia: permite mapear niveles de energía, induce estados cuánticos colectivos, perfila colores, brillos y transparencias, y hace visibles las estructuras espaciales y los movimientos internos. Ya estemos diseñando un dispositivo que juega con sombras y destellos, analizando una molécula por espectroscopía o imaginando un procesador cuántico de fotones superfluidos, estamos usando las mismas leyes físicas que gobiernan esas minúsculas vibraciones de electrones y núcleos bajo la acción de un campo electromagnético oscilante.

