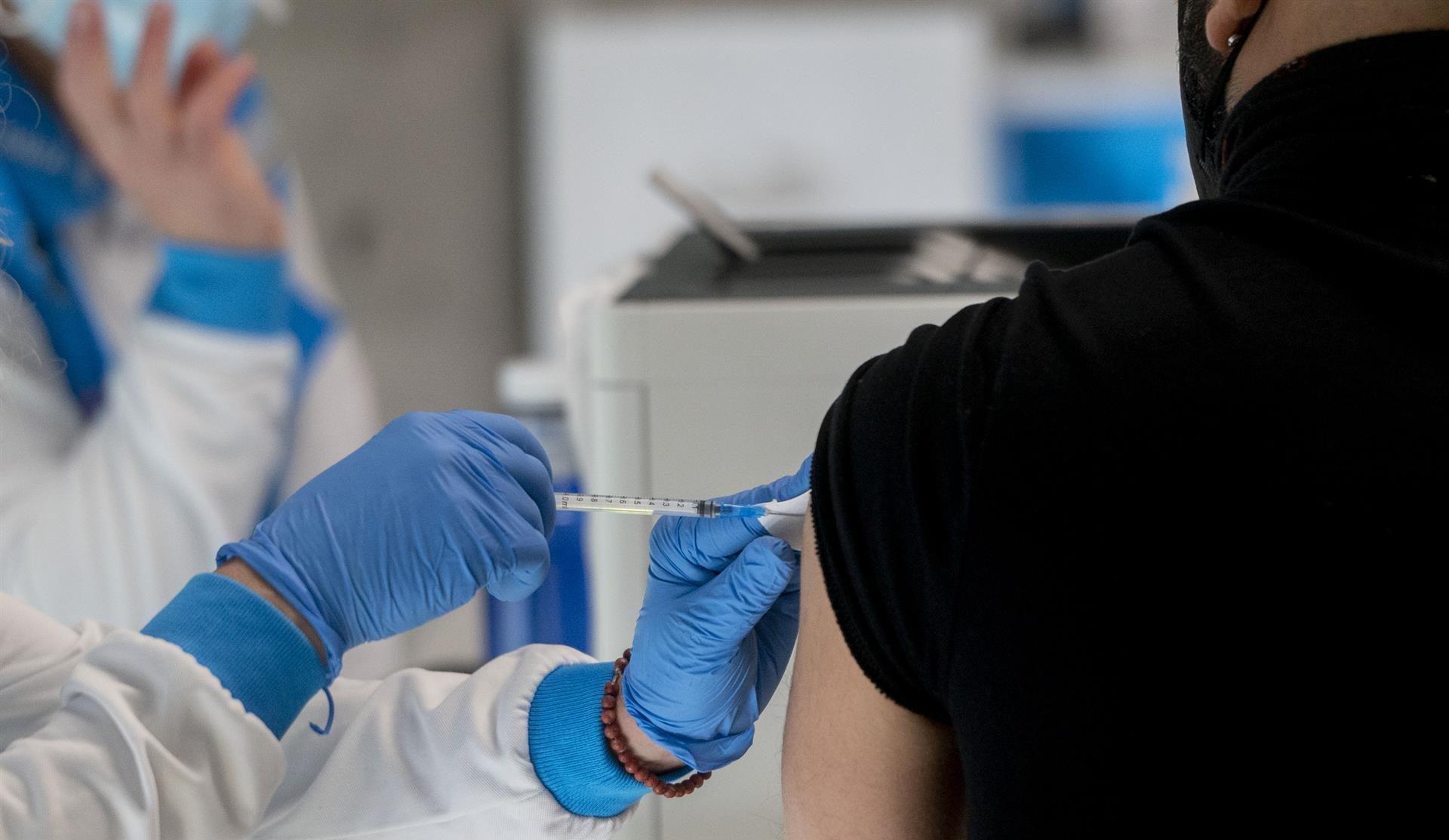
- Las vacunas reducen infecciones, consumo de antibióticos y la presión selectiva que impulsa la resistencia antimicrobiana.
- La OMS estima que las vacunas actuales podrían evitar más de 100.000 muertes por RAM y millones de días de antibióticos al año.
- Vacunas ya consolidadas (Hib, neumococo, gripe) y nuevas en desarrollo (C. difficile, S. aureus, TB) son clave en los planes frente a RAM.
- Integrar la vacunación en las estrategias One Health y en los planes nacionales de RAM es esencial para preservar la eficacia de los antibióticos.

La resistencia a los antimicrobianos (RAM) se ha convertido en una de las grandes amenazas sanitarias del siglo XXI. Cada año causa cientos de miles de muertes en el mundo, un enorme gasto sanitario y pérdidas millonarias en productividad. Frente a este escenario tan preocupante, las vacunas han pasado de ser vistas solo como una herramienta para prevenir infecciones concretas a considerarse una pieza clave en la estrategia global contra las bacterias resistentes.
Aunque durante años el discurso sobre RAM se ha centrado casi en exclusiva en el uso racional de antibióticos, el control de infecciones y la vigilancia microbiológica, hoy está claro que sin una política de vacunación ambiciosa y bien integrada en los planes nacionales será imposible frenar el problema. Las evidencias científicas acumuladas, los informes de la OMS y el posicionamiento de sociedades científicas españolas apuntan todos en la misma dirección: si se utilizan bien las vacunas, se reduce de forma muy notable el consumo de antibióticos y, con ello, la aparición y diseminación de resistencias.
Magnitud del problema de las resistencias a los antibióticos
La carga global de la resistencia bacteriana es abrumadora. En un análisis de 2019, se estimó que, de 7,7 millones de muertes asociadas a 33 infecciones bacterianas diferentes, alrededor de 5 millones podrían atribuirse directamente a la resistencia a los antibióticos. No hablamos solo de fallecimientos: también de discapacidad, secuelas a largo plazo, estancias hospitalarias más largas y tratamientos mucho más caros.
Los informes recientes de la OMS y grupos de expertos internacionales calculan que, si nada cambia, la RAM podría causar hacia mediados de siglo más de 10 millones de muertes anuales, superando incluso al cáncer. Actualmente, se calcula que al menos 700.000 personas mueren cada año por infecciones resistentes, una cifra que ya supera con creces las muertes combinadas por tétanos, cólera y sarampión.
En Europa, se estiman unas 35.000 muertes anuales por RAM, y en España, en torno a 4.000 muertes cada año se relacionan con esta problemática. A ello se suman costes sanitarios adicionales que, solo en nuestro entorno, se cuentan en cientos de millones de euros, sin incluir la pérdida de productividad por bajas laborales, secuelas o incapacidad.
El origen del problema es multifactorial: se abusa de los antibióticos en medicina humana, se prescriben para infecciones virales o cuadros leves en los que no son necesarios, se interrumpen tratamientos antes de tiempo, se usan antibióticos de amplio espectro sin indicación clara y, además, se emplean masivamente en la ganadería y otros ámbitos para promover el crecimiento de animales o prevenir infecciones en condiciones de alta densidad.
La lista de patógenos prioritarios elaborada por la OMS incluye bacterias con niveles de resistencia especialmente altos, como Escherichia coli, Klebsiella pneumoniae, Enterobacter spp., Pseudomonas aeruginosa, Acinetobacter baumannii, Staphylococcus aureus resistente a meticilina o cepas multirresistentes de Mycobacterium tuberculosis. Todas ellas son responsables de infecciones graves (neumonías, sepsis, infecciones urinarias complicadas, meningitis, infecciones postquirúrgicas) y, en muchos casos, ya apenas responden a los antibióticos disponibles.
El papel estratégico de la OMS: vacunas frente a resistencias antimicrobianas
La Organización Mundial de la Salud ha dado un giro claro en la última década al incorporar de manera explícita a las vacunas dentro de sus estrategias contra la RAM. En 2020 publicó el marco de acción “Leveraging Vaccines to Reduce Antibiotic Use and Prevent Antimicrobial Resistance”, donde se explican las principales vías por las que la inmunización puede disminuir el uso de antibióticos y la propagación de cepas resistentes.
Más recientemente, la OMS ha desarrollado un extenso informe técnico que analiza el impacto cuantificable de las vacunas sobre la resistencia a los antimicrobianos y el consumo de antibióticos. En ese documento se evalúan 44 vacunas (en uso o en investigación) dirigidas contra 24 patógenos distintos: 19 bacterias, cuatro virus (gripe, norovirus, rotavirus y virus respiratorio sincitial, VRS) y un parásito (Plasmodium falciparum, causante principal de la malaria).
Este análisis contempla varias dimensiones: reducción de muertes, años de vida ajustados por discapacidad (DALYs), disminución del uso de antimicrobianos, ahorro económico en hospitalizaciones y reducción de pérdidas de productividad. Además, distingue entre vacunas ya implantadas, vacunas en fases clínicas avanzadas con alta probabilidad de aprobación, y otras en fases más tempranas con probabilidad media o baja de llegar a usarse de manera rutinaria.
Según las estimaciones de la OMS, las vacunas que ya están en los calendarios, usadas con coberturas adecuadas, podrían evitar cada año unas 106.000 muertes asociadas a RAM, junto con 9,1 millones de DALYs, más de 860 millones de dólares en costes de hospitalización y cerca de 5.900 millones en productividad perdida. Además, permitirían reducir alrededor de 142 millones de dosis diarias definidas (DDD) de antibióticos al año.
Si, además, se alcanzaran los objetivos de la Agenda de Inmunización 2030 (IA2030), por ejemplo aumentando la cobertura de vacunación neumocócica en la infancia y en las personas mayores, se podrían evitar aproximadamente 27.000 muertes adicionales anuales, con el consiguiente ahorro sanitario y social.
Clasificación de las vacunas según su potencial frente a la RAM
La OMS agrupa las 44 vacunas analizadas en tres grandes categorías según su estado de desarrollo y la probabilidad de uso amplio: vacunas ya en uso o con alta probabilidad de aprobación, vacunas con probabilidad media de llegar a los programas y vacunas con probabilidad baja.
En el primer bloque se incluyen las vacunas frente a Streptococcus pneumoniae (neumococo), Mycobacterium tuberculosis, Salmonella Typhi, Haemophilus influenzae tipo b (Hib), Neisseria gonorrhoeae, Plasmodium falciparum, rotavirus y el VRS (ya sea mediante vacunas o anticuerpos monoclonales de larga duración). Entre ellas, neumococo, tuberculosis y fiebre tifoidea aparecen como las que mayor impacto global podrían tener en muertes evitadas, uso de antibióticos y costes económicos.
En el segundo grupo, de probabilidad media, se sitúan candidatas frente a E. coli extraintestinal, Klebsiella pneumoniae, estreptococo del grupo A, Shigella, E. coli enteropatógena, Pseudomonas aeruginosa, Salmonella no tifoidea, Campylobacter jejuni, Helicobacter pylori y norovirus. No todas muestran un impacto elevado en los modelos, pero varias de ellas podrían reducir de forma significativa cuadros diarreicos y septicemias que hoy se tratan masivamente con antibióticos.
Por último, en el grupo de probabilidad baja de aprobación se agrupan múltiples proyectos aún en fases tempranas. Algunas formulaciones mejoradas contra E. coli extraintestinal, neumococo y Staphylococcus aureus tendrían un potencial enorme si se aplicaran en población infantil, personas mayores y grupos de riesgo, ya que se centran en patógenos muy relacionados con el consumo intensivo de antibióticos y la aparición de cepas multirresistentes.
El informe subraya que, aunque los beneficios estimados para las vacunas aún en investigación están rodeados de una mayor incertidumbre, el margen de mejora es tan grande que merece la pena considerarlas dentro de la planificación estratégica y de las prioridades de inversión en I+D.
Mecanismos por los que las vacunas reducen la resistencia
Las vacunas contribuyen a frenar la RAM a través de varios mecanismos complementarios, algunos muy directos y otros más sutiles. En conjunto, generan una reducción clara de la presión selectiva que los antibióticos ejercen sobre las bacterias.
En primer lugar, la vacunación disminuye las infecciones causadas por los propios patógenos incluidos en la vacuna, ya sean cepas sensibles o resistentes. Es el caso, por ejemplo, de las vacunas conjugadas antineumocócicas que han reducido de forma drástica la enfermedad invasora causada por serotipos de S. pneumoniae, muchos de ellos asociados a resistencia a penicilina y otros antibióticos. Menos infecciones se traduce en menos tratamientos antibióticos.
En segundo lugar, varias vacunas reducen el riesgo de complicaciones bacterianas tras infecciones virales frecuentes. La gripe es el ejemplo típico: la inmunización antigripal disminuye los episodios de neumonía bacteriana secundaria y otitis media, procesos que en muchos casos requerirían antibióticos. Lo mismo ocurre con las vacunas frente a COVID-19 o frente al VRS en lactantes, que reducen significativamente las hospitalizaciones por bronquiolitis y otras infecciones respiratorias donde, en la práctica, a menudo se pautan antibióticos de forma empírica.
Un tercer mecanismo es la llamada inmunidad de grupo o inmunidad comunitaria. Al cortar cadenas de transmisión y reducir la circulación de un patógeno en la población, también se protegen indirectamente personas no vacunadas o con respuesta inmune insuficiente. Este efecto se ha visto con particular claridad en las vacunas conjugadas frente a Hib y neumococo, donde la caída de la colonización nasofaríngea ha ido acompañada de un descenso importante de las cepas resistentes en la comunidad.
Además, al disminuir la incidencia de infecciones virales respiratorias y gastrointestinales, las vacunas ayudan a reducir un problema muy habitual en la práctica clínica: la prescripción innecesaria de antibióticos ante cuadros febriles en los que no se dispone de diagnóstico rápido. Vacunas como las de rotavirus, varicela o la propia antigripal han demostrado reducir visitas médicas, ingresos y tratamientos antimicrobianos injustificados.
Por último, al limitar la circulación de patógenos se reducen las oportunidades de intercambio de genes de resistencia (por ejemplo, mediante plásmidos) entre bacterias, así como la presión evolutiva que favorece la selección de cepas multirresistentes. Aunque este aspecto es más complejo de medir, los modelos epidemiológicos y los datos de vigilancia microbiológica apuntan a que el efecto es real y relevante a medio y largo plazo.
Resultados cuantitativos de la OMS: qué impacto pueden tener las vacunas
Los modelos de la OMS no se han limitado a hacer una reflexión teórica, sino que han generado cifras concretas de impacto en distintos escenarios. En términos de muertes evitadas atribuibles a RAM, la vacuna (o combinación de vacunas) frente a la tuberculosis aparece como la herramienta con mayor potencial, seguida de las dirigidas a Klebsiella pneumoniae, E. coli extraintestinal, neumococo y Staphylococcus aureus.
La distribución geográfica del beneficio tampoco es homogénea. El análisis por regiones de la OMS indica que el continente africano sería el territorio donde la introducción y mejora de la cobertura de estas vacunas tendría el mayor impacto, con casi 200.000 muertes anuales evitadas. La explicación es clara: mayor carga de enfermedad infecciosa, menor acceso a antibióticos de calidad y más barreras para el diagnóstico temprano.
Un caso especialmente interesante es el del virus respiratorio sincitial (VRS) en lactantes. La estrategia de vacunación materna o el uso de anticuerpos monoclonales de larga duración (como nirsevimab) no solo reduce ingresos hospitalarios y mortalidad infantil, sino que se asocia a una importante disminución del consumo de antibióticos en todo el mundo, dada la gran cantidad de exploraciones respiratorias que terminan tratándose empíricamente con antimicrobianos.
Para las vacunas actualmente en uso, las estimaciones combinadas apuntan a que podrían evitar 106.000 muertes, millones de DALYs y un volumen considerable de hospitalizaciones cada año, con ahorros superiores a los 6.000 millones de dólares al sumar costes sanitarios directos y productividad. Aplicado a la práctica, esto equivale a menos camas ocupadas, menos terapias de alto coste, menos complicaciones y menos familias afectadas.
Para las vacunas en fases avanzadas o tempranas de desarrollo, el impacto potencial llega a cifras aún mayores (centenares de miles de muertes evitadas), si bien sujeto a las incertidumbres propias del desarrollo clínico, los cambios en la epidemiología y los niveles de cobertura vacunal que realmente se consigan en el mundo real.
Vacunas ya probadas que reducen la resistencia a los antibióticos
Más allá de los modelos, existen ejemplos muy sólidos de vacunas que ya han demostrado en la práctica su capacidad para frenar la RAM. Uno de los casos paradigmáticos es la vacuna conjugada frente a Haemophilus influenzae tipo b (Hib). Su introducción en calendarios infantiles de numerosos países produjo una caída casi total de la enfermedad invasora y una reducción significativa en las cepas productoras de β-lactamasas, lo que se tradujo en menos necesidad de antibióticos de amplio espectro.
Algo parecido ha ocurrido con las vacunas conjugadas neumocócicas (VNC). La primera generación (VNC7) y las posteriores (VNC10, VNC13 y formulaciones aún más amplias) han conseguido disminuir de forma muy marcada la enfermedad neumocócica invasora en menores de cinco años y también en adultos, gracias a la inmunidad de grupo. En apenas siete años tras la introducción de VNC7 en 2000, se estimó que se habían evitado más de 200.000 casos de enfermedad invasora en todas las edades, y los aislamientos resistentes a penicilina descendieron en paralelo.
En España se ha documentado una clara disminución de la resistencia a penicilina en cepas pediátricas de neumococo tras la introducción de la vacuna conjugada, especialmente en aislamientos de sangre y líquido cefalorraquídeo. Algo similar se ha visto en otros países europeos dentro de los sistemas de vigilancia como EARSS, lo que refuerza el mensaje de que la vacunación puede modificar de forma tangible el panorama de resistencias.
Las vacunas antigripales ofrecen otro ejemplo interesante. Al reducir la incidencia de gripe, se limita la aparición de complicaciones bacterianas que suelen tratarse con antibióticos (neumonías, sobreinfecciones respiratorias, otitis). Pero, además, se ha observado una bajada en las prescripciones inadecuadas de antibióticos para cuadros respiratorios de origen viral, lo que representa un beneficio doble en términos de RAM.
También se han acumulado datos sobre el efecto de vacunas frente a diarrea (como rotavirus) en la reducción del uso de antibióticos en la infancia, especialmente en entornos con recursos limitados, donde cualquier cuadro diarreico severo suele tratarse con antimicrobianos de forma empírica ante la imposibilidad de hacer diagnósticos rápidos.
Vacunas en desarrollo con alto potencial frente a RAM
El pipeline de vacunas dirigidas a patógenos con gran capacidad para desarrollar resistencias es cada vez más amplio. Destacan varios proyectos en fases clínicas avanzadas que, de llegar al mercado, podrían tener un impacto enorme en la reducción del uso de antibióticos.
Entre ellos, se sitúan las vacunas contra Clostridioides difficile, principal causa de diarrea nosocomial asociada al uso de antibióticos en países industrializados. El CDC la considera una amenaza urgente. Dos candidatos vacunales se encuentran en fase 3 de ensayos clínicos, centrados en adultos de 50 años o más, que son quienes sufren mayor incidencia y gravedad. Si se consiguiera prevenir una parte significativa de estos episodios, no solo habría menos morbimortalidad, sino también menos ciclos repetidos de antibióticos de amplio espectro y menos transmisión de cepas hipervirulentas.
Otro frente es el de las vacunas contra Staphylococcus aureus, incluyendo cepas resistentes a meticilina (SAMR). Este patógeno causa infecciones invasoras graves y un porcentaje muy alto de infecciones quirúrgicas. La aparición de resistencia a glucopéptidos como la vancomicina genera especial preocupación, ya que estos antibióticos son de los pocos recursos que quedan frente a SAMR. Existen varias vacunas en fases 1-2/3, como SA4Ag o 4C-Staph, orientadas a prevenir infecciones en pacientes quirúrgicos u otros grupos de riesgo.
El estreptococo del grupo B (SGB) es otro objetivo prioritario. Coloniza el tracto genital y rectal de muchas mujeres y puede causar sepsis y meningitis neonatal. Hoy en día, la estrategia principal es la antibioterapia intraparto, que expone tanto a la madre como al recién nacido a antibióticos (incluidos macrólidos y vancomicina en caso de alergias o resistencias). Las vacunas conjugadas frente a SGB, administradas en el embarazo, buscan generar anticuerpos maternos que se transfieran al feto y protejan al recién nacido, reduciendo así la necesidad de profilaxis antibiótica masiva.
En el ámbito de las enterobacterias multirresistentes, se están explorando vacunas frente a E. coli uropatógena y K. pneumoniae, dos de los principales culpables de infecciones urinarias y bacteriemias en todo el mundo. Una vacuna eficaz frente a E. coli uropatógena podría evitar millones de tratamientos antibióticos por infecciones urinarias no complicadas cada año, con el consiguiente efecto sobre la RAM.
Por último, el desarrollo de nuevas vacunas frente a Mycobacterium tuberculosis es un campo de trabajo intensísimo. La BCG actual protege bien a la infancia frente a formas graves de TB, pero no impide la reactivación de la infección latente ni corta de forma clara la transmisión pulmonar en adultos. Dado que alrededor del 5 % de los nuevos casos de TB son multirresistentes y los tratamientos son largos, tóxicos y caros, una vacuna más efectiva tendría un impacto dramático en las cifras globales de RAM.
Posicionamiento de sociedades científicas y enfoque One Health
En España, la Asociación Española de Vacunología (AEV) ha sido muy clara al reivindicar el papel de las vacunas como aliadas clave en la lucha contra la resistencia a los antibióticos. En sus aportaciones al Proyecto de Real Decreto del Plan Estratégico frente a la RAM, la AEV insiste en que cualquier estrategia nacional debe integrar objetivos específicos relacionados con la vacunación.
Entre sus propuestas destacan: fomentar la introducción de vacunas esenciales en el calendario oficial, mejorar las coberturas vacunales para maximizar el impacto preventivo, incluir el efecto sobre RAM en los estudios de coste-efectividad de nuevas vacunas, reforzar la vigilancia de la resistencia vinculada a las inmunizaciones y crear un registro nacional de hospitalizaciones y muertes asociadas a RAM.
En paralelo, iniciativas como el proyecto “Prevención y Salud Global, pilares para un futuro sostenible”, impulsado por ECODES y Pfizer, subrayan el enfoque One Health (Una sola salud), que integra salud humana, animal y ambiental. En este marco, las vacunas se consideran una de las herramientas más poderosas para recortar en torno a un 22 % el consumo actual de antibióticos, tal y como ha señalado el profesor Bruno González-Zorn a partir de estimaciones de la OMS.
Expertos de distintas sociedades científicas —pediatría, medicina de familia, enfermedades infecciosas, microbiología, salud pública— coinciden en que falta aún concienciación tanto en la población como entre algunos profesionales sanitarios sobre el doble beneficio de las vacunas: previenen la enfermedad inmediata y reducen riesgos asociados, como eventos cardiovasculares tras gripe o reactivaciones oncológicas, y al mismo tiempo contribuyen a preservar la eficacia futura de los antibióticos.
El decálogo elaborado en ese proyecto incluye acciones prácticas para la ciudadanía: vacunarse (incluyendo a las mascotas cuando corresponda), lavarse las manos con frecuencia, evitar la automedicación, completar siempre los tratamientos antibióticos pautados, desechar los sobrantes en puntos SIGRE y consultar solo fuentes fiables de información. Son medidas aparentemente sencillas pero con un impacto enorme sobre la circulación de patógenos y el desarrollo de resistencias.
Retos pendientes y prioridades en políticas públicas
A pesar de las evidencias, la cobertura vacunal sigue siendo subóptima en muchos contextos. Incluso en países de renta alta, las tasas de vacunación antigripal en personal sanitario rondan apenas un tercio, y hay lagunas en la vacunación de riesgo (embarazadas, crónicos, mayores). En países de renta baja y media, se añaden barreras logísticas, falta de financiación y problemas de acceso.
La OMS y distintos grupos de expertos recomiendan integrar de forma explícita en los planes nacionales contra la RAM una serie de elementos relacionados con vacunas: metas concretas de coberturas, seguimiento del impacto en consumo de antibióticos, inversión en investigación de nuevas vacunas dirigidas a patógenos prioritarios, y licencias y despliegue simultáneos en países de distintos niveles de renta.
Otra recomendación clave es incorporar indicadores de RAM en los propios programas de inmunización. No basta con medir coberturas y efectividad frente a la enfermedad diana; es necesario monitorizar también métricas como: días de tratamiento antibiótico evitados, reducción de prescripciones en atención primaria y hospitalaria, descenso en la proporción de aislamientos resistentes en los sistemas de vigilancia microbiológica.
Además, se reclama una colaboración mucho más estrecha entre programas de vacunación, equipos de uso prudente de antibióticos, servicios de microbiología y unidades de control de infecciones. Compartir datos, diseñar estudios conjuntos y analizar de forma integrada la información clínica, microbiológica y vacunal permitiría entender mejor cómo se relacionan las campañas de inmunización con la evolución de la RAM.
Por el lado de la innovación farmacéutica, el panorama de nuevos antibióticos no es especialmente alentador: en los últimos años, el número de moléculas en desarrollo clínico ha caído, y la mayoría pertenecen a familias ya conocidas, con solo un puñado capaces de actuar frente a bacterias extremadamente resistentes. De ahí que muchos expertos subrayen que cada dosis de antibiótico que podamos evitar gracias a una vacuna es, en la práctica, un pequeño seguro de vida para la eficacia futura de estos fármacos.
Tomando todo esto en conjunto, el mensaje central es que las vacunas han dejado de ser un simple “complemento” en la lucha contra la resistencia antimicrobiana para convertirse en uno de sus pilares. Incrementar la vacunación a lo largo de toda la vida, invertir en nuevas vacunas dirigidas a patógenos prioritarios, medir su impacto en uso de antibióticos y coordinarlas con el resto de intervenciones es una estrategia imprescindible si queremos que los antibióticos sigan funcionando para las próximas generaciones.